|
|
|
高考化学必考知识点《化学平衡常数》考点强化练习(2017年押题版)(二)
2017-09-25 19:18:17
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
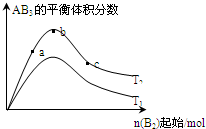
1、选择题 某化学科研小组研究在其它条件不变时,改变某一条件对A2(g)+3B2(g)

2AB3(g)化学平衡状态的影响时,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据图示得出的结论中正确的是( )
A.反应速率a>b>c
B.达到平衡时A2的转化率大小为:a>b>c
C.若T2>T1,则正反应一定是放热反应
D.达到平衡时,AB3的物质的量大小为:c>b>a
| 
参考答案:D
本题解析:
本题难度:简单
2、选择题 |
|
参考答案:AC
本题解析:
本题难度:简单
3、选择题 已知448℃时反应H2(g)+I2(g)?2HI(g)的平衡常数是49,则HI(g)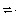 1/2H2(g)+1/2I2(g)?,在该温度下的平衡常数是( )
1/2H2(g)+1/2I2(g)?,在该温度下的平衡常数是( )
A.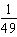
B.2401
C.7
D.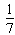
参考答案:D
本题解析:
本题难度:简单
4、填空题 在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)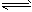 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表

回答下列问题:
(1)该反应的化学平衡常数表达式为K=_________。
(2)该反应为_________反应(选填“吸热”、“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是_________(多选扣分)。
a.容器中压强不变
b.混合气体中c(CO)不变
c.υ正(H2)=υ逆(H2O)
d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)・c(H2)=c(CO)・c(H2O),试判断此时的温度为
_________℃。
参考答案:(1)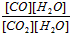
(2)吸热
(3)bc
(4)830
本题解析:
本题难度:一般
5、填空题 Ⅰ.描述弱电解质电离情况可以用电离度(电离度:一定条件下,当弱电解质达到电离平衡时,溶液中已电离的电解质分子数占原电解质分子总数的百分数)和电离平衡常数表示,下表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb),表2是常温下几种难(微)溶物的溶度积常数(Ksp)。
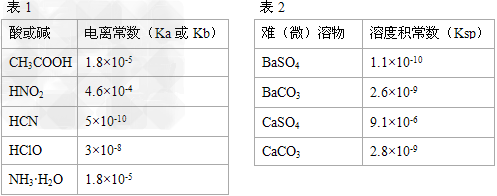
请回答下面问题:
⑴下列能使醋酸溶液中CH3COOH的电离度增大,而电离常数不变的操作是_______(填序号)。
A.升高温度?B.加水稀释? C.加少量的CH3COONa固体?D.加少量冰醋酸
⑵CH3COONH4的水溶液呈______(选填“酸性”、“中性”、“碱性”),理由是____________________。
⑶工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如:BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使c(SO42-?)达到0.0l?mol/L以上,则溶液中c(CO32-?)应≥_______?mol/L。
Ⅱ.化学在能源开发与利用中起着重要的作用,如甲醇、乙醇、二甲醚(CH3OCH3)等都是新型燃料。
⑴乙醇是重要的化工产品和液体燃料,可以利用下列反应制取乙醇。
2CO2(g)+6H2(g)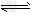 CH3CH2OH(g)+3H2O(g)?△H=a?kJ/mol 在一定压强下,测得上述反应的实验数据如下表。
CH3CH2OH(g)+3H2O(g)?△H=a?kJ/mol 在一定压强下,测得上述反应的实验数据如下表。
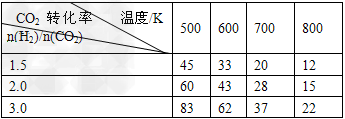
根据表中数据分析:
①上述反应的?a_______0(填“大于”或“小于”)。
②在一定温度下,提高氢碳(即n(H2)/n(CO2)?)比,平衡常数K值_______(填“增大”、“减小”、或“不变”),对生成乙醇______(填“有利”或“不利”)。
⑵催化剂存在的条件下,在固定容积的密闭容器中投入一定量的CO和H2,同样可制得乙醇(可逆反应)。该反应过程中能量变化如图所示:
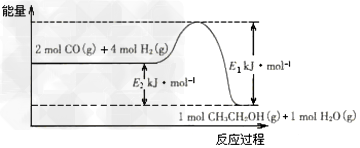
①写出CO和H2制备乙醇的热化学反应方程式_________________。
②在一定温度下,向上述密闭容器中加入1?mol?CO、3?mol?H2及固体催化剂,使之反应。平衡时,反应产生的热量为Q?kJ,若温度不变的条件下,向上述密闭容器中加入4?mol?CO、
12?mol?H2及固体催化剂,平衡时,反应产生的热量为w?kJ,则w的范围为___________。
⑶二甲醚(CH3OCH3)被称为21世纪的新型燃料,具有清洁、高效的优良性能。以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池,其工作原理与甲烷燃料电池原理相类似。该电池中负极上的电极反应式是_________________。
参考答案:Ⅰ⑴B;⑵中性;水电离出的H+和OH-的浓度相等,CH3COONH4溶于水后,根据电离平衡常数,CH3COO-结合H+和NH4+结合OH-生成弱电解质的程度一样,导致水溶液中的H+和
OH-浓度相等,呈中性;⑶0.24
Ⅱ⑴①小于;②不变;有利
?⑵①2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g)? △H=-E2 kJ・mol-1;?②4Q<w<2E2
CH3CH2OH(g)+H2O(g)? △H=-E2 kJ・mol-1;?②4Q<w<2E2
⑶CH3OCH3-12e-+16OH-=2CO32-+ 11H2O
本题解析:
本题难度:困难
