1������� �Ա���Ϊȼ����������ȼ�ϵ�أ���ص�����ͨ��O2��CO2������ͨ����飬�����������̼���Ρ���ط�Ӧ����ʽΪ _____________________________________________________���ŵ�ʱCO32�������ص�____________�����������������
�ο��𰸣�C3H8��5O2=3CO2��4H2O����
���������
�����Ѷȣ�һ��
2��ѡ���� ��п��صij��ͷŵ���̿ɱ�ʾΪ�� 2Ag+Zn(OH)2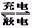 Ag2O+Zn+2H2O���˵�طŵ�ʱ�������Ϸ�����Ӧ��������(? )
Ag2O+Zn+2H2O���˵�طŵ�ʱ�������Ϸ�����Ӧ��������(? )
A��Ag
B��Zn(OH)2
C��Ag2O
D��Zn
�ο��𰸣�D
�������������ԭ��ع���ԭ���������Ϸ���������Ӧ.Ԫ�ػ��ϼۻ����ߣ������ڷŵ�����б���������Zn����ZnΪ����.
�����Ѷȣ�һ��
3��ѡ����
|
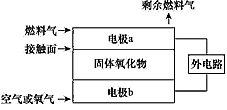
����������ȼ�ϵ�أ�SOFC���Թ�����������Ϊ����ʣ�O2-���������ڲ�����ͨ�����乤��ԭ����ͼ��ʾ�����й��ڹ���ȼ�ϵ�ص��й�˵����ȷ����
[? ]
A���缫bΪ��ظ������缫��ӦʽΪO2+4e-==2O2-
B��������������������õ����ڵ����ͨ��
C����H2��Ϊȼ��������Ӵ����Ϸ����ķ�ӦΪH2+2OH-��4e-==2H++H2O
D����C2H4��Ϊȼ��������Ӵ����Ϸ����ķ�ӦΪC2H4+6O2-��12e-==2CO2+2H2O
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� ��6�֣��״�(CH3OH)�Ͷ����ѣ�CH3OCH3������Ϊ21���͵�����ȼ�ϡ���CH4��H2OΪԭ���Ʊ��״��Ͷ����ѵĹ�ҵ�������£�
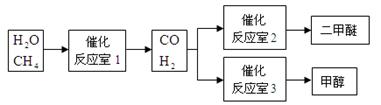
����Ҫ��ش��������⣺
��1������Ӧ��1����һ�������·�Ӧ�Ļ�ѧ����ʽΪ ��
��2��ˮú���ϳɶ����ѵ�������Ӧ���£�
��2H2(g)+CO(g) CH3OH(g) ��H = -90.8kJ��mol-1
CH3OH(g) ��H = -90.8kJ��mol-1
��2CH3OH(g) CH3OCH3(g)+H2O(g) ��H = -23.5kJ��mol-1
CH3OCH3(g)+H2O(g) ��H = -23.5kJ��mol-1
��CO(g)+H2O(g) CO2(g)+H2(g) ��H = -41.3kJ��mol-1
CO2(g)+H2(g) ��H = -41.3kJ��mol-1
����Ȼ�ѧ��Ӧ����ʽ��3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)����H = ��
CH3OCH3(g)+CO2(g)����H = ��
��3��ij���л������Ƶ�һ�����͵����ӽ���Ĥ������ȼ�ϵ��(DDFC)���õ���нϸߵİ�ȫ�ԡ��õ���ܷ�ӦΪCH3OCH3+3O2=2CO2+3H2O���乤��ԭ����ͼ��ʾ��
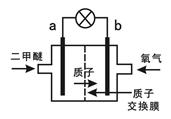
�缫a�ĵ缫��ӦʽΪ ��
�ο��𰸣���1��CH4+H2O CO+3H2 ��2�֣���2��-246.4kJ��mol-1��2�֣���λ���÷֣�
CO+3H2 ��2�֣���2��-246.4kJ��mol-1��2�֣���λ���÷֣�
��3��CH3OCH3-12e-+3H2O 2CO2+12H+��2�֣�
2CO2+12H+��2�֣�
�����������1��������ͼ����CH4��H2O�ڴ����������·�Ӧ������ CO��H2����ѧ����ʽΪ��CH4+H2O CO+3H2 ��2���١�2+��+�ۿɵ��ܷ�Ӧ����H =-90.8��2-23.5-41.3=-246.4kJ��mol-1[����3����ȼ�ϵ���У�ȼ�Ϸ�Ӧ��һ���Ǹ�����������Ӧ��һ��������������a�Ǹ���,ʧȥ���ӣ��缫��ӦΪ��CH3OCH3-12e-+3H2O
CO+3H2 ��2���١�2+��+�ۿɵ��ܷ�Ӧ����H =-90.8��2-23.5-41.3=-246.4kJ��mol-1[����3����ȼ�ϵ���У�ȼ�Ϸ�Ӧ��һ���Ǹ�����������Ӧ��һ��������������a�Ǹ���,ʧȥ���ӣ��缫��ӦΪ��CH3OCH3-12e-+3H2O 2CO2+12H+[
2CO2+12H+[
���㣺����������д��ѧ����ʽ���Ȼ�ѧ����ʽ�ļ��㡢ȼ�ϵ�ص缫��Ӧ����д��
�����Ѷȣ�����
5��ѡ���� �������طŵ�ʱ���ܷ�ӦʽΪFe+Ni2O3+3H2O�TFe��OH��2+2Ni��OH��2�������йظõ�ص�˵����ȷ���ǣ�������
A����صĸ���ΪNi2O3������ΪFe
B����صĵ��Һ�����Ǽ�����Һ��Ҳ������������Һ
C����طŵ�ʱ��������ӦʽΪNi2O3+3H2O+2e-�T2Ni(OH)2+2OH-
D����س��ʱ������������Һ��pH����
�ο��𰸣�A���ɷŵ�ʱ�ķ�Ӧ���Եó�������ԭ��ʧȥ���ӣ�Ni2O3���������õ����ӣ�������ΪNi2O3������ΪFe����A����
B�����ݷŵ�ʱ�ܷ�Ӧ����ʽ֪�������Ϊ����������Ե�صĵ��ҺӦ��Ϊ������Һ����B����
C����طŵ�ʱ�������ϵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪNi2O3+3H2O+2e-=2Ni��OH��2+2OH-����C��ȷ��
D�����ʱ����ʧ���ӷ���������Ӧ���缫��ӦʽΪ��2Ni��OH��2+2OH--2e-=Ni2O3+3H2O����������������Һ��pH���ͣ���D����
��ѡC��
���������
�����Ѷȣ�һ��