1、填空题 (3分)浓度均为0.1 mol/L的溶液:①HNO3;②H2SO4;③CH3COOH;④Ba(OH)2;?⑤NaOH;⑥CH3COONa;⑦KCl;⑧NH4Cl;⑨NH3・H2O;⑩NaHCO3;溶液的pH由小到大的顺序是:?。(填编号)
参考答案:②①③⑧⑦⑥⑩⑨⑤④
本题解析:硝酸是一元强酸,硫酸是二元强酸,醋酸是一元弱酸,氢氧化钡是二元强碱,氢氧化钠是一元强碱,醋酸钠水解显碱性,氯化钾显中性,氯化铵水解显酸性,氨水是一元弱碱,碳酸氢钠到水解程度大于醋酸钠的,显碱性,所以pH由小到大到顺序是②①③⑧⑦⑥⑩⑨⑤④。
本题难度:简单
2、计算题 在25 ℃时,有pH为x的盐酸和pH为y的NAOH溶液,取Vx L该盐酸同该NAOH溶液中和,需Vy L NAOH,求:
(1)若x+y=14时,则Vx/Vy=_______________(填数值)。
(2)若x+y=13时,则Vx/Vy=_______________(填数值)。
(3)若x+y>14时,则Vx/Vy=_______________(填表达式),且VxVy____________(填“>”“=”或“<”)。
参考答案:(1)1?(2)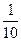 (3)10x+y-14?>
(3)10x+y-14?>
本题解析:因为pH="x?" c(H+)=10-x mol・L-1
pH="y?" NaOH中pOH="14-y?" c(OH-)=10-(14-y)=10y-14
H+? +? OH-====H2O
10-x×Vx? 10y-14×Vy
所以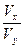 =
=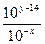 =10x+y-14
=10x+y-14
本题难度:简单
3、选择题 25℃时向10V mL pH=a的盐酸中,滴加pH=b的NaOH溶液V mL时,溶液中Cl-物质的量恰好等于加入的Na+的物质的量,则a+b的值为(?)
A.15
B.14
C.13
D.不能确定
参考答案:A
本题解析:溶液中Cl-物质的量恰好等于加入的Na+的物质的量,说明二者恰好反应,溶液显中性。所以10×10-a=1×10b-14,则a+b=15,答案选A。
本题难度:一般
4、选择题 室温下,把1 mL 0.1 mol・L-1的H2SO4加水稀释成2 L溶液,在此溶液中由水电离产生的H+,其浓度接近于
A.1×10-4 mol・L-1
B.1×10-8 mol・L-1
C.1×10-11 mol・L-1
D.1×10-10 mol・L-1
参考答案:D
本题解析:略
本题难度:一般
5、选择题 下列事实能说明甲酸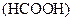 属于弱酸的是(? )
属于弱酸的是(? )
①1mol/LHCOOH的pH=2
②甲酸能与水以任意比互溶
③20mL 1mol/LHCOOH与20mL 1mol/LNaOH恰好中和
④HCOONa溶液的pH>7
A.①②
B.②③
C.③④
D.①④
参考答案:
D
本题解析:
弱酸是弱电解质,不能完全电离,①中1mol/LHCOOH的pH=2说明HCOOH部分电离,所以①可以证明HCOOH是弱酸。②说的是甲酸的溶解度,与电解质的强弱无关。③只能说明HCOOH是一元酸,与强弱无关。④HCOONa溶液的pH>7,说明HCOO―水解显碱性,根据“谁弱谁水解”,则证明HCOOH是弱酸。所以①④可以证明HCOOH是弱酸,D正确。
本题难度:简单