1、简答题 I.市场上出售的“热敷袋”,其主要成分是铁屑、碳粉、木屑与少量氯化钠、水等.它在使用之前需用塑料袋与空气隔绝.使用时启开塑料袋上的气孔,轻轻揉搓就会放出热量来.当使用完后还会发现有铁锈生成.依上述现象回答:
(1)碳粉的主要作用是______.
(2)加入氯化钠的作用是______.
(3)试写出上述变化过程中负极的电极反应式,负极:______.
Ⅱ.将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计.若该电池中两电极的总重量为60g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47g,试计算:产生氢气的体积(标准状况).(要写计算过程)
参考答案:I.(1)碳粉和铁活泼性不同,且都导电;氯化钠是强电解质,易溶于水;碳粉、铁、氯化钠溶液构成了原电池,碳的活泼性比铁小,所以作正极,因为形成原电池,从而加速铁的氧化.
故答案为:与铁、氯化钠溶液构成原电池,碳作电池的正极,从而加速铁的氧化
(2)氯化钠是强电解质,易溶于水,溶于水后得到电解质溶液,
故答案为:氯化钠溶于水形成电解质溶液.
(3)、铁的活泼性大于碳的,在构成的原电池中,铁作负极,铁失去电子变成离子进入溶液,
故答案为:Fe-2e-=Fe2+.
Ⅱ.银片和锌片分别作原电池的正负极,当发生反应时,负极材料失电子变成离子进入溶液,质量减少;正极材料不参加反应,所以本题质量减少的量是锌的质量.
锌减少的质量为60g-47g=13g,结合方程式计算生成氢气的体积.
Zn+H2SO4=ZnSO4 +H2↑
65g 22.4L
13g 4.48L
答:产生氢气的体积为4.48L.
本题解析:
本题难度:一般
2、选择题 有4种金属a,b,c,d,将c置于a的盐溶液中,放出气体 且生成c的氢氧化物,若b,d做电极,插入硝酸银溶液中组成原电池,在b上析出银;若a,d相接触放在空气中,a先腐蚀。则4种金属的活动性由强到弱的顺序是
[? ]
A.b>d>a>c
B.c>a>d>b
C.c>b>a>d
D.d>c>a>b
参考答案:B
本题解析:
本题难度:一般
3、填空题 某课外活动小组同学用右图装置进行实验,一段时间后在C电极表面有铜析出,试回答下列问题.
(1)A为电源的______极;
(2)E的电极反应式为:______;
(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为______;
(4)在常温下,现用丙装置给铁镀铜,则H电极材料应该是______,当丙中铁表面析出铜的3.2g时,乙中溶液的PH值为______(假设溶液体积为1L);
(5)在电解一段时间后在甲中加入适量______可以使溶液恢复到原来的浓度.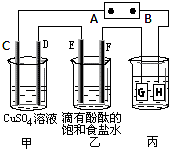
参考答案:(1)C电极上有铜析出,C电极上发生还原反应,所以C电极是阴极,连接阴极的是负极,所以A为负极,故答案为:负极.
(2)C是阴极,则D是阳极,E是阴极,F是阳极,阳离子在阴极上发生还原反应,溶液中氢离子的放电能力大于钠离子,所以氢离子放电,故答案为:2H++2e-=H2↑
(3)根据离子的放电顺序判断,甲、乙装置中C、D、E、F四个电极上分别生成的物质是Cu、O2、H2、
Cl2,根据得失电子数相等,这四种物质间的关系式为?2Cu--O2--2 H2--2Cl2,根据物质的量之比等于计量数之比知,物质的量之比为2:1:2:2,故答案为:2:1:2:2.
(4)根据题意知,G为阴极,H为阳极;根据电镀原理,镀层在阳极,镀件在阴极,所以H电极材料应该是铜;
乙装置中的氢气来源于水,一个水分子电离成一个氢离子和一个氢氧根离子,两个氢离子生成一个氢分子,所以氢分子和氢氧根离子的关系式为? H2 --2 OH?-;根据得失电子数相等,丙装置中析出的铜与乙装置中氢气的关系式为
? Cu--H2;所以氢氧根离子和铜的关系式为?
? ? Cu--2 OH?-
? 64g?2mol?
? 3.2g? 0.1mol
?所以C(OH-)=0.1 mol/L,则C(H+)=1×10-13?mol/L,所以PH=13,故答案为:铜;13;
(5)甲装置中电解反应方程式为 2CuSO4+2H2O?电解?.?2Cu+O2↑+2H2SO4
由方程式知,电解出的物质有铜和氧气,所以加入氧化铜即可,故答案为:CuO(若考虑到水开始电解Cu(OH)2也可以)
本题解析:
本题难度:一般
4、选择题 将炭粉和铁粉均匀混合,撒入内壁分别用氯化钠溶液和稀醋酸溶液润湿过的具支试管中,并按下图装置好仪器,观察下图,示意正确的是(?)

A? B? C? D
参考答案:B
本题解析:略
本题难度:简单
5、填空题 从能量转化的角度看,原电池是一种由_______能转变成________能的装置;用锌片、铜片和稀盐酸组成的原电池,负极是________,正极的电极反应是___________________,正极发生 反应(填“氧化”或“还原”)
参考答案:化学 电 Zn 2H+ + 2 e- =" " H2 ↑ 还原
本题解析:略
本题难度:一般