1、简答题 某研究性学习小组查阅资料得知:漂白粉与硫酸溶液反应可制取氯气,化学方程式为:Ca(C1O)2+CaCl2+H2SO4
2CaSO4+2Cl2↑+2H2O,该组学生针对上述反应设计如下装置来制取氯气并验证其性质.

试回答下列问题:
(1)每生成1mol?Cl2,上述化学反应中转移的电子个数为______?(NA表示阿伏加德罗常数).
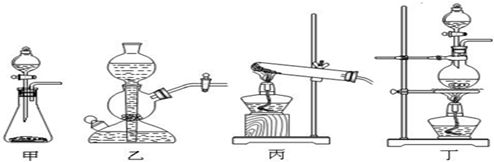
(2)该实验中A处可选用装置______(填写甲.乙.丙或丁).
(3)检查A装置的气密性的方法是用弹簧夹夹住______处(填a.b.c或d)橡皮管,向分液漏斗中加水并打开活塞,当加到一定量时,停止加水,静止观察,当观察到分液漏斗中______?时,表明该装置不漏气.
(4)装置B中发生反应的离子方程式为______.
(5)装置C中发生反应的离子方程式为______
(6)装置E中的试剂是______(任填一种合适试剂的名称),其作用是______
(7)请帮助该学习小组同学设计一个实验,证明装置D中有FeCl3生成(请简述实验步骤)______.
参考答案:(1)Ca(C1O)2+CaCl2+H2SO 4??△?.?2CaSO4+2Cl2↑+2H2O? 转移电子
?2?mol? 2 NA?
? 1mol? NA?
故答案为:NA?
(2)反应物的状态为固体和液体,反应条件是加热.
故选丁.
(3)夹住橡皮管,向分液漏斗中加水并打开活塞,如果漏气,分液漏斗内压强减小,水面会下降,否则不含下降.
故答案为:a,液面(水面)不下降.
(4)漏气有氧化性,能置换出碘单质,
故答案为:Cl2+2I-=I2+2Cl-
(5)氯气有氧化性,亚硫酸钠有还原性,氯气和亚硫酸钠能发生氧化还原反应,生成硫酸钠和盐酸.
故答案为:Cl2+SO32-+H2O=SO42-+2H++2Cl-
(6)氯气有毒,不能直接排空,因为氯气和水反应生成盐酸和次氯酸,酸能和碱反应,从而达到吸收氯气的作用.故答案为:氢氧化钠溶液或碳酸钠溶液;?吸收多余的氯气,防止污染空气.
(7)三价铁离子和硫氰化钾反应,使溶液变成血红色.
故答案为:取装置D中的溶液于一支洁净试管中,滴加适量的KSCN溶液,溶液变成血红色,则证明有FeCl3生成.
本题解析:
本题难度:一般
2、实验题 在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间)。下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。
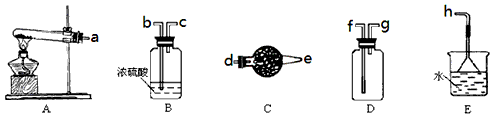
(1)实验室制取、收集干燥的NH3,需选用上述仪器装置的接口连接顺序是(选填字母):a接______,
______接______,______接h;用A装置制取NH3的化学反应方程式为__________________
(2)用下图所示装置也可以制取NH3,则圆底烧瓶中的固体可以选用______(选填字母编号);
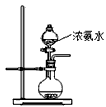
A.碱石灰 B.生石灰 C.无水氯化钙 D.无水硫酸铜 E.烧碱
(3)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是______,试写出制纳米级碳酸钙的化学方程式__________________;
(4)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级__________________。
参考答案:(1)d;e;g;f;2NH4Cl+Ca(OH)2 CaCl2 + 2NH3↑+ H2O
CaCl2 + 2NH3↑+ H2O
(2)ABE
(3)NH3;CaCl2+CO2+2NH3+H2O=CaCO3↓+2NH4Cl
(4)取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级碳酸钙,否则不是
本题解析:
本题难度:一般
3、实验题 实验室用下列有关装置先制取干燥、纯净的Cl2并进行漂白性性质实验,试根据下列装置回答有关问题。
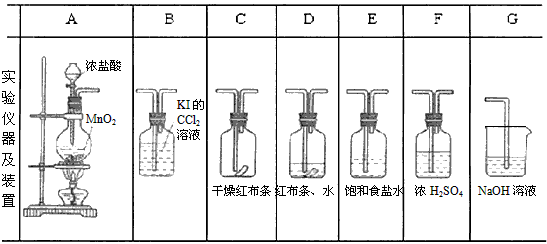
(1)上述装置中各仪器从左至右的连接顺序是_______________________。
(2)E装置目的是_______________________,D装置是为了_______________________,
(3)分别写出A、G中的化学反应原理______________________________________________
参考答案:(1)A、E、F、C、D、B、G
(2)除去HCl;做对比参照实验
(3)MnO2+4HCl(浓) MnCl2+Cl2+2H2O,Cl2+2NaOH==NaCl+NaClO+H2O
MnCl2+Cl2+2H2O,Cl2+2NaOH==NaCl+NaClO+H2O
本题解析:
本题难度:一般
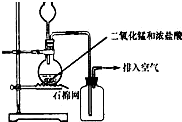
4、简答题 如图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置.其中D瓶中放有干燥红色布条;E中为铜网,E右端出气管口附近为石棉球.

试回答:
(1)A中发生反应的方程式为______;
(2)为得到干燥纯净的氯气,一般在B瓶中加入饱和食盐水,其作用是______;
(3)C中盛放的试剂为______;D处看到的现象是______;
(4)E中所发生反应的方程式为______.
(5)F中应加入的试剂为______,其作用是______.
(6)若A中有14.6gHCl被氧化,将产生的氯气通入足量的KI溶液中能产生单质碘的质量为______g.
参考答案:(1)实验室是利用二氧化锰和浓盐酸加热反应生成氯气,A中是浓盐酸,B中是二氧化锰固体,反应的化学方程式为MnO2+4HCl(浓)△.MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)△.MnCl2+Cl2↑+2H2O;
(2)生成的氯气中含有氯化氢,用饱和食盐水除去氯气中的氯化氢,故答案为:吸收HCl气体;
(3)用浓硫酸除去氯气中的水蒸气得到干燥纯净的氯气;干燥的氯气遇到干燥有色布条不褪色,说明氯气无漂白作用,
故答案为:浓H2SO4;红色布条不褪色;
(4)E是铜加热和氯气反应生成氯化铜的反应,生成的氯化铜形成棕色烟,反应的化学方程式为:Cu+Cl2△.CuCl2,故答案为:Cu+Cl2=CuCl2;
(5)氯气有毒,不能排放到空气中,需要用氢氧化钠溶液吸收,氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:氢氧化钠溶液;吸收多余的氯气;
(6)若A中有14.6g HCl被氧化,n(HCl)=将产生的氯气通入足量的KI溶液中能产生单质碘的质量=14.6g36.5g/mol=0.4mol,
MnO2+4HCl(浓)△.MnCl2+Cl2↑+2H2O;Cl2+2KI=I2+2KCl,反应中被氧化2molHCl生成1molCl2,1molCl2和碘化钾反应生成碘单质1mol
则定量计算关系为:2HCl~Cl2~I2
2 1
0.4mol 0.2mol
得到碘单质质量=0.2mol×254g/mol=50.8g;
故答案为:50.8g.
本题解析:
本题难度:一般
5、简答题 某化学小组用如图所示装置制取氯气.下列说法不正确的是( )
A.该装置图中至少存在三处明显错误
B.该实验中收集氯气的方法不正确
C.为了防止氯气污染空气,必须进行尾气处理
D.在集气瓶的导管口处放一片湿润的淀粉碘化钾试纸可以证明是否有氯气逸出