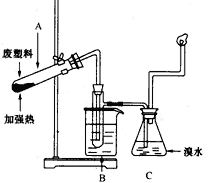
1、实验题 某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如下图所示。 加热聚丙烯废塑料得到的产物如下表所示:
 ?
? 
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔。 A中残留物聚乙炔写出反应②、③的化学方程式_____________;____________ 。
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有__________ 种。
(3)锥形瓶C中观察到的现象是____________ ,经溴水充分吸收后,剩余气体经干燥后平均相对分子质量为________________ 。
(4)写出C中逸出的气体在工业上的两种用途___________ 、___________。
参考答案:
(1)CaC2+2H2O→Ca(OH)2+C2H2 ;CH≡CH→
(2)4
(3)棕黄色溶液变无色(或溴水褪色);4.8
(4)合成氨原料; 作燃料或有机化工原料
本题解析:
本题难度:一般
2、简答题 某校学生课外活动小组的同学设计如下图所示实验装置,用来验证一氧化碳具有还原性.回答下列问题:

(1)装置B中最适宜的试剂是______,其作用是______
(2)装置C的作用是______,若实验中没有装置C,则不可以证明CO具有还原性,原因是:______
(3)装置D中黑色固体为______,反应的化学方程式为______
(4)根据实验中的______现象,可证明CO具有还原性,有关反应的化学方程式是______
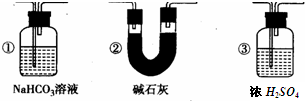
(5)若要根据装置F中出现的现象确认一氧化碳具有还原性,应在上图装置______与______之间连接图中的______装置(填序号).
参考答案:(1)实验室用盐酸和石灰石制取二氧化碳,该反应放出的热量导致盐酸挥发,所以制取的二氧化碳中含有氯化氢气体,为除去氯化氢气体,选取的试剂应能除去氯化氢气体且不和二氧化碳反应,则只能选取可溶性的饱和碳酸氢盐,一般
常用饱和的碳酸氢钠溶液,故答案为:饱和碳酸氢钠溶液,除去CO2混有的HCl;
(2)浓硫酸具有吸水性,且和二氧化碳不反应,所以能干燥二氧化碳;若实验中没有装置C,从B装置出来的气体中含有水蒸气,碳和水蒸气反应生成的氢气也能还原氧化铜,从而造成干扰,
故答案为:干燥CO2,C和H2O反应生成的H2也能还原氧化铜;
(3)高温条件下,二氧化碳和碳反应生成一氧化碳,所以D装置中的黑色固体是碳,反应方程式为:CO2+C?高温?.?2CO,
故答案为:C,CO2+C?高温?.?2CO;
(4)一氧化碳具有还原性,所以能还原黑色的氧化铜,使其变为红色的铜单质,所以E中的现象是:黑色固体变为红色,反应方程式为:CO+CuO?△?.?Cu+CO2,
故答案为:E中黑色固体变红,CO+CuO?△?.?Cu+CO2;?
(5)和二氧化碳的反应中,二氧化碳不可能完全转化为一氧化碳,所以从D装置出来的气体中含有二氧化碳,为防止原来二氧化碳的干扰,应先把D出来的二氧化碳除去,再将一氧化碳气体通过E装置,二氧化碳是酸性氧化物,所以用碱性物质除去,所以选②,故答案为:D、E,②.
本题解析:
本题难度:一般
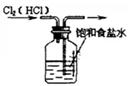
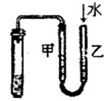
3、选择题 如图所示的实验中,能达到实验目的的是
| 
| 
| 
|
①除去Cl2中的HCl杂质
| ②用铜和稀硝酸制取少量NO
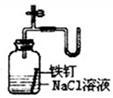
| ③证明铁生锈时空气参与反应
| ④检验装置气密性
|
?
A.①②③④? B.③④? C.②③④? D.①④
参考答案:B
本题解析:氯化氢极易溶于水,则除去Cl2中的HCl杂质可以选择饱和食盐水,但应该是长口进,短口出,①不正确;NO极易被氧化生成NO2,所以不能用排空气法收集,②不正确;实验③中铁生锈时如果空气参与反应,则U形瓶中但液面会发生变化,据此可以判断,③正确;根据检验装置气密性的方法可知,选项④正确,答案选B。
点评:化学实验常用仪器的使用方法和化学实验基本操作是进行化学实验的基础,对化学实验的考查离不开化学实验的基本操作,所以该类试题主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。
本题难度:一般
4、实验题 (14分)已知硝酸锏溶液颜色为蓝色.某学校化学课外小组同学们在做铜与浓硝酸、稀硝酸反应的实验中,发现铜和浓硝酸反应后溶液为绿色旦有红棕色气体产生,而铜和稀硝酸反应后溶液为蓝色,产生无色气体.为弄清反应后溶液颜色出现差异的原因,他们进行了实验探究.
[实验]在两支试管中各放入一小块等质量的铜片,分别加人等体积的浓HN03(14 mol ?
L-1)和稀HN03(4mol . L-1 ), 立即用蘸有NaOH的棉花封住试管口。充分反应后铜均无剩余。
(1) Cu与浓HNO3反应的离子方程式________________________________
(2) 用蘸有NaOH的棉花封住试管口的原因________________
已知NO2与NaOH溶液反应中,其中NO2的还原产物是亚硝酸盐(NO2-)
写出反应的化学反应式________________________,
[提出假设]假设一、因为铜离子浓度大造成的。
假设二、溶液呈绿色是因为铜与浓硝酸反应时产生的二氧化氮溶于过量浓硝酸,加上和蓝色的硝酸铜溶液混在一起,使溶液呈绿色。
[设计实验方案,验证假设]
(3) 上述实验________(“能”或“不能”)证明假设一不成立,原因________________
(4) 甲同学设计实验验证假设二,请帮他完成下表中内容(提示:NO3-在不同条件下的还咬产物较复杂,有时难以观察到气体产生)

[分析推理】
(5)铜和稀硝酸反应后溶液为蓝色的原理________________
参考答案:(14分)

本题解析:略
本题难度:一般
5、实验题 已知过氧化钠与水的反应分两步进行,第一步是过氧化钠与水反应生成过氧化氢和氢氧化钠;第二步是过氧化氢分解生成水和氧气。某校合作学习探究小组对过氧化钠与水的反应进行了再探究。将过氧化钠与一定量的水反应,有气泡放出,将所得的浓溶液分成四份,分别进行实验探究:

试回答:
(1)按要求写出下列反应的化学方程式:
①过氧化钠与水反应生成过氧化氢和氢氧化钠:_______________________________。
②在二氧化锰作用下过氧化氢发生分解反应:_______________________________。
(2)根据B、D两个实验,回答D实验中酚酞试液不变红的原因是_____________________________。
(3)综合考虑,回答A实验中酚酞试液不变红的原因可能是:
①_______________________;②_________________________。
参考答案:(1)①Na2O2+2H2O==2NaOH+H2O2;②2H2O2 2H2O+O2↑
2H2O+O2↑
(2)H2O2有漂白性(或强氧化性)
(3)H2O2有漂白性(或强氧化性);NaOH的浓度大或OH-的浓度大
本题解析:
本题难度:困难