1�������� ��10 g������40 mLijŨ�ȵ������У����ȳ�ַ�Ӧ���ռ���1792 mL������壬��Һ�ﻹ����4.4 g���壨��״��������
��1����Ӧ����ԭ��������δ����ԭ����������ʵ���
��2��ԭ������Һ�����ʵ���Ũ��
��3������������ɳɷּ��������
�ο��𰸣�
�����������
�����Ѷȣ�һ��
2��ѡ���� ��100 mLϡ�����ϡ����Ļ������Һƽ���ֳ����ݡ�������һ��������ͭ�ۣ�������ܽ�9��6g�������ʱ����ֻ����ԭΪNO����ͬ��������һ�����������ۣ�����������������������ı仯��ͼ��ʾ�������жϴ�����ǣ�?��
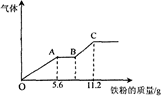
A��OA�����������NO��BC�����������H2
B��A���Ӧ����NO3�����ʵ���Ϊ0��1 mol
C��B���Ӧ���������۵�����Ϊ8��4 g
D��ԭ�������Һ��H2SO4Ũ��Ϊ2��0 mol��L��1
�ο��𰸣�D
���������A��OA��Fe+4H++NO3-��Fe3++NO��+2H2O
AB��Fe+2Fe3+��? 3Fe2+
BC��Fe+2H+��? Fe2++H2��
B����������ӵ�����������ɸ�������ͭ�����ó�
���ݵ�ʧ�����غ㣺0.15��2=x��3���ó�NO3�����ʵ���Ϊ0.1mol
C������ͼ��AB�Ρ�OA�η�Ӧԭ���ɵ�B���Ӧ���������۵�����Ϊ8��4 g
D������Ԫ�������غ㣬��������ȫת��ΪFeSO4������H2SO4�����ʵ���Ϊ0.2mol,��ԭ���Һ�е�Ũ��Ϊ0.2/0.05=4��0 mol��L��1
�����Ѷȣ�һ��
3�������� ��12�֣���1����Ũ�����з���ͭƬ��
�ٿ�ʼ��Ӧ�Ļ�ѧ����ʽΪ___________________________________
����ͭ��ʣ�࣬��Ӧ��Ҫ����ʱ�ķ�Ӧ�����ӷ���ʽ��?��
�۴���Ӧֹͣ���ټ���������25%��ϡ���ᣬ��ʱͭƬ���������ݲ�������ԭ����
_____________________________________________________��
(2) ��100mL������У�c��HNO3�� = 0��4mol��L-1��c��H2SO4�� = 0��2mol��L-1�������м���2��56gͭ�ۣ��ȣ�����ַ�Ӧ����Һ��Cu2�������ʵ���Ũ��Ϊ?��
��3��14gͭ���Ͻ��������ijŨ�ȵ�������Һ��Ӧ�����ų���������1.12L����״���£��������ͨ��ˮ�У�ǡ��ȫ����ˮ���գ���Ͻ���ͭ��������?��
�ο��𰸣�(12��)
��1���� Cu + 4HNO3��Ũ��= Cu��NO3��2 + 2NO2�� + 2H2O ��2�֣�
��3Cu + 8H�� + 2NO3�� =3Cu2�� + 2NO�� + 4H2O��2�֣�
���ټ���ϡH2SO4��H����NO3�D������������������2�֣�
��2��0.15mol��L-1?��3�֣�
��3��3��2g��3�֣�
�����������1��ͭ�����ᷴӦ����Ũ���йأ�
Cu + 4HNO3��Ũ��= Cu��NO3��2 + 2NO2�� + 2H2O
3Cu + 8HNO3��ϡ��="3" Cu��NO3��2 + 2NO�� + 4H2O
�۴���Ӧֹͣ���ټ���������25%��ϡ�����ṩH������Һ�е�NO3���ɼ�������ͭ
��2��NO3����H����Cu��Ϊ0��04mol�������������ӷ���ʽ��
3Cu ?+ ?8H��?+?2NO3�� =3Cu2�� + 2NO�� + 4H2O
0.015mol? 0.04mol? 0.01mol? 0.015mol
��Һ��Cu2�������ʵ���Ũ��Ϊ0.15mol��L-1
(3)��Ͻ���ͭΪx mol����Ϊ y mol
�ɺϽ�������֪��64x+108y=14?�ɵ����غ�ɵã�2x+y=4��11.2/22.4
x=0.05mol? y=0.1mol
����ͭΪ3��2g
�����Ѷȣ�һ��
4��ѡ���� ���з�Ӧ�У�����ȱ������ԣ��ֱ��������Ե���(? )
A��Fe(OH)2��ϡ���ᷴӦ
B��Fe2O3��ϡ���ᷴӦ
C��CuO��ϡ���ᷴӦ
D��Al(OH)3��ϡ���ᷴӦ
�ο��𰸣�A
���������A���ܽ�Ϊ���ԣ����������Ϊ�����ԣ�
BCD�����ϼ�û�иı䣬ֻ������
�����Ѷȣ�һ��
5�������� �������������������ŷų����ķ����к���NO��NO2��������Ⱦ���������а�����ԭ��������ת��Ϊ������(������)_____ֱ���ŷſ����У�д���йط�Ӧ����ʽ��______������NO��NO2���ʵ���________֮��ǡ��Ϊ1��1�������ߵĻ�����൱��һ��������д�����ռ���Һ�������������Ļ�ѧ����ʽ��________��
�ο��𰸣�������6NO2+8NH3 7N2+12H2O
7N2+12H2O
6NO+4NH3 5N2+6H2O
5N2+6H2O
NO+NO2+2NaOH====2NaNO2+H2O
��(N2O3+2NaOH====2NaNO2+H2O)
������������۵ĵ��Ļ������븺�۵ĵ��Ļ������������Է�����Ӧ���ɵ���N2������NO2��NH3�ڴ�����������������N2���ʡ�
�ڶ��գ�NO��NO2���ʵ���֮��Ϊ1��1�Ļ����൱������������N2O3������N�Ļ��ϼ�Ϊ+3�ۣ���NaOH��Һ��Ӧ��������Ӧ�ļ�̬���κ�ˮ����Ӧʽ��N2O3+2NaOH====2NaNO2+H2O
�����Ѷȣ�һ��