1、选择题 有关氨气的实验较多,下面对这些实验原理的分析中,正确的是
A.氨气极易溶于水,可以用来做喷泉实验
B.氨气的还原性可以解释氨气与氯化氢的反应实验
C.NH3・H2O不稳定,实验室可用NH4Cl和石灰水制取氨气
D.NH3液化时放出大量的热,因而,不能用氨作制冷剂
参考答案:A
本题解析:略
本题难度:简单
2、选择题 14gCu、Ag合金与足量某浓度的硝酸反应,将放出的气体与1.12L O2(标况)混合,恰好能被水全部吸收生成硝酸,则合金中Cu的质量为
A.1.6g
B.3.2g
C.6.4g
D.9.6g
参考答案:B
本题解析:设合金中铜和银的物质的量分别是x、y。根据题意可知,该过程发生的化学反应有:铜和硝酸反应、硝酸的还原产物和氧气的反应又生成硝酸。铜、银和硝酸反应时金属失去电子,硝酸根离子得到电子生成气体氮的氧化物,氮的氧化物和氧气、水反应生成硝酸时,氮的氧化物失去电子氧气得到电子,这说明实质上得失电子物质为氧气和金属。1.12L O2(标况)的物质的量是1.12L÷22.4L/mol=0.05mol,所以转移电子的物质的量为0.05mol×4=0.2mol。则根据电子得失守恒可知2x+y=0.2,根据质量守恒可知64x+108y=14,解得x=0.05mol、y=0.1mol,所以合金中铜的质量为0.05mol×64g/mol=3.2g,答案选B。
本题难度:一般
3、选择题 下列各组物质互为同素异形体的是(?)
A.红磷和白磷
B.磷酸和偏磷酸
C.NO2和N2O4
D.35Cl和37Cl
参考答案:A
本题解析:同种元素组成的不同单质,不是化合物,也不是原子。
本题难度:简单
4、选择题 在标准状况下,将NO、NO2、O2三种气体按一定比例充满一固定容积的容器,并将该容器倒置在水槽中,充分反应后,容器中无气体剩余,所得溶液的浓度为Mmol/L。则M的取值范围是
A.0<M<1/22.4
B.1/39.2<M<1/22.4
C.1/28<M<1/22.4
D.1/39.2<M<1/28
参考答案:D
本题解析:设烧瓶容积为V升,采用极值法
当原混合气体全部为NO和O2时:4NO+3O2+2H2O=4HNO3,硝酸的物质的量为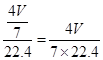 =mol,溶液的浓度为
=mol,溶液的浓度为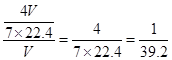 =mol/L
=mol/L
当原混合气体全部为NO2和O2时:4NO2+O2+2H2O=4HNO3,硝酸的物质的量为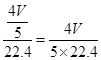 =mol,溶液的浓度为
=mol,溶液的浓度为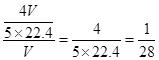 mol/L
mol/L
故答案为D
本题难度:一般
5、选择题 汽车排放出的尾气中含有NO2,是城市大气主要污染物之一,在日光照射下,NO2发生一系列化学烟雾的循环反应,从而不断产生O3,加重空气污染。反应过程为:①NO2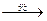 NO+O;②2NO+O2====2NO2;③O+O2====O3,下列对该反应过程的有关叙述正确的是(?)
NO+O;②2NO+O2====2NO2;③O+O2====O3,下列对该反应过程的有关叙述正确的是(?)
A.NO2起催化剂作用
B.NO起催化剂作用
C.NO2只起氧化剂作用
D.O3的氧化性比O2的氧化性弱
参考答案:A
本题解析:NO2参加反应但反应前后质量没变,即为催化剂。
本题难度:简单