1、选择题 常温下,在下列各组溶液中,加水稀释时c(OH-)/c(H+)的值明显增大,且能大量共存的离子组是(?)。
①K+、Al3+、NO3-、AlO2-
②K+、Fe2+、I-、SO42-
③K+、I-、NO3-、Na+
④Na+、Ca2+、Al3+、Cl-
A.①②
B.①③
C.②④
D.②③
参考答案:C
本题解析:由题意知加水稀释时c(OH-)/c(H+)的值明显增大,可知该溶液显酸性。①中Al3+和AlO2-不能大量共存;③中溶液显中性。②中Fe2+水解,④中Al3+水解,使溶液呈酸性,且离子间不发生反应,所以正确选项为C。
本题难度:一般
2、选择题 下列离子能大量共存而且溶液为无色透明的是( )
A.NH4+、Al3+、SO42-、NO3-
B.Cu2+、Na+、NO3-、CO32-
C.Na+、K+、OH-、Mg2+
D.H+、K+、HCO3-、CO32-
参考答案:A.溶液无色,且离子之间不发生任何反应,能大量共存,故A正确;
B.Cu2+有颜色,不符合溶液要求,故B错误;
C.OH-与Mg2+反应生成沉淀而不能大量共存,故C错误;
D.H+与HCO3-、CO32-反应,都生成二氧化碳气体,不能大量共存,故D错误.
故选A.
本题解析:
本题难度:简单
3、填空题 pC类似pH,是指极稀溶液中,溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为1×10-3mol・L-1,则该溶液中溶质的pC=-lg(1×10-3)=3。下图为,H2CO3在加入强酸或强碱溶液后,平衡时溶液中三种成分的pC―pH图。请回答下列问题:
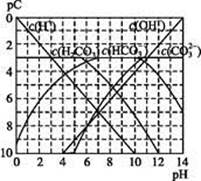
(1)在人体血液中, 能起到使人体血液pH保持在7.35~7.45的作用。①请用电解质溶液中的平衡解释: (用离子方程式表示)。?
能起到使人体血液pH保持在7.35~7.45的作用。①请用电解质溶液中的平衡解释: (用离子方程式表示)。?
②正常人体血液中, 的水解程度 电离程度(填“<”“>”或“=”)。?
的水解程度 电离程度(填“<”“>”或“=”)。?
③pH=7.00的血液中,c(H2CO3) c( )(填“<”“>”或“=”)。?
)(填“<”“>”或“=”)。?
(2)H2CO3一级电离平衡常数的数值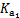 ≈ 。?
≈ 。?
(3)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的C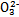 不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确。?
不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确。?
(4)已知某温度下Li2CO3的Ksp为1.68×10-3,将适量Li2CO3固体溶于100 mL水中至刚好饱和,饱和Li2CO3溶液中c(Li+)="0.15" mol・L-1.c(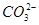 )="0.075" mol・L-1。若t1时刻在上述体系中加入100 mL 0.125 mol・L-1 Na2CO3溶液,列式计算说明是否有沉淀产生。
)="0.075" mol・L-1。若t1时刻在上述体系中加入100 mL 0.125 mol・L-1 Na2CO3溶液,列式计算说明是否有沉淀产生。
参考答案:(1)①
 H++
H++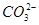 .
. +H2O
+H2O H2CO3+OH- ②> ③<
H2CO3+OH- ②> ③<
(2)1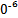
(3)用pH试纸(或pH计)测常温下0.1 mol・L-1 Na2CO3溶液的pH,若pH<12,该同学的观点正确;若pH>12,则该同学的观点错误
(4)c(Li+)="0.075" mol・L-1.c(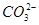 )="0.1" mol・L-1,
)="0.1" mol・L-1,
c2(Li+)・c(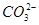 )=5.6×1
)=5.6×1 <1.68×10-3,所以无沉淀产生。
<1.68×10-3,所以无沉淀产生。
本题解析:(1)①依据信息抓住 既能水解也能电离分析;②由信息可知正常人体血液显碱性,所以水解大于电离;③由图像可知c(H2CO3)=c(
既能水解也能电离分析;②由信息可知正常人体血液显碱性,所以水解大于电离;③由图像可知c(H2CO3)=c( )时溶液显酸性,显中性时c(
)时溶液显酸性,显中性时c( )>c(H2CO3);(2)
)>c(H2CO3);(2)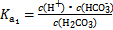 ,pH=6时c(H2CO3)=c(
,pH=6时c(H2CO3)=c( ),所以
),所以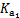 =c(H+);(3)由
=c(H+);(3)由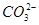 +H2O
+H2O
 +OH-可知测一定浓度的Na2CO3溶液中c(OH-)即可求出已水解的Na2CO3的浓度;(4)注意最后溶液的体积为原体积的2倍。
+OH-可知测一定浓度的Na2CO3溶液中c(OH-)即可求出已水解的Na2CO3的浓度;(4)注意最后溶液的体积为原体积的2倍。
本题难度:一般
4、选择题 下列离子在指定溶液中一定能大量共存的是
A.能使甲基橙变红的溶液中:Fe2+、Al3+、NO3-、Cl-、S2-
B.在pH=11的溶液中:Na+、AlO2-、NO3-、S2-、SO32-
C.室温下,由水电离的c(H+)=10-10mol/L的溶液中:Cl-、HCO3-、NO3-、NH4+、F-
D.加入Mg能放出H2的溶液中:Mg2+、NH4+、ClO-、K+、SO42-