1��ѡ���� �й�AgCl�������ܽ�ƽ��˵����ȷ����
[? ]
A��AgCl�������ɺͳ����ܽ�����ʶ�������
B��AgCl������ˮ����Һ��û��Ag+��Cl-
C����AgCl�����м���NaCl���壬AgCl�������ܶȻ���Ksp������
D�������¶ȣ�AgCl�������ܽ�Ȳ���
2������� ij�����ķ�ˮ�к���FeSO����H��SO����Ag��SO����Al�ˣ�SO����3��һЩ���࣮ij�о���ѧϰ������ⶨ�˷�ˮ�и����ʵĺ������������ܽ�����ݣ����б����£�
��һ��ˮ�и����ʵĺ���
| ���� | FeSO�� | H��SO�� | Ag��SO�� | Al�ˣ�SO������ | ����
��������/��%��
15.��
7.��
��.����
��.3��
5.��
|
����?FeSO����Al�ˣ�SO����3��ˮ�е��ܽ��
| �¶�/�� | �� | 1�� | ���� | 3�� | ���� | 5��
FeSO����Һ�ȣ�g��
15.6
����.5
��6.5
3��.9
����.��
��8.6
Al�ˣ�SO����3�ܽ�ȣ�g��
31.��
33.5
36.��
����.��
��5.7
5��.��
|
�ÿ�������ݱ������ݣ��������ˮ���������������øó��ķ���м����������ߣ����ռ���Һ�����ᴦ������ˮ������FeSO��?7H��O��Ag��
��1������д���пհף���ɵõ�Ag��ʵ�鷽����
�ٽ�������ߵķ���м�Ⱥ����ȵ��ռ���Һ����ˮ����ϴ�ӣ�Ŀ����______��
�ڽ�������ˮ���ˣ�������ˮϴ��������ϴ��Һ������Һ�������ã�
��______��Ŀ����ʹAg+ȫ����ԭΪ����Ag��
��______��Ŀ���Ƿ����Ag��
���ˣ���д�������IJ��裬��ȥAl3+���õ���Ҫ�ɷ�ΪFeSO��?7H��O���壮
�ݽ���______����ڢܲ�������Һ��Ϻ����������������Һ��pHΪ3-����______���˳�FeSO��?7H��O����
��3��д������������л�ѧ��Ӧ�����ӷ���ʽ______��
�������ڲ�����У����������������pH��Ŀ����______��
3������� ��֪Ksp(PbCrO4)=2.8��10-13 mol2��L-2, Ksp(CaCrO4) =7.1��10-4 mol2��L-2����Pb2+ ��Ca2+�Ļ����Һ
��Pb2+ ��Ca2+��Ũ�Ⱦ�Ϊ0. 10 mol��L-1���еμ�K2 CrO4�� Һ������ֳ����Ĵ���Ϊ__________��
4��ѡ���� �±��г��˼��ֳ������ʵĵ��볣�����ܶȻ���

��һ������0.2 mol��L CaCl2��Һ�м���������������Һ�����Բ�����������(? )
A����ˮ�������c(H��)=10��9 mol/L��HF��Һ
B��pH��10�İ�ˮ
C��1 mol��L��NaHCO3��Һ
D��10-9 mol��L��AgNO3��Һ
5��ѡ���� ��ˮ�к��зḻ��þ��Դ��ijͬѧ����˴�ģ�⺣ˮ���Ʊ�MgO��ʵ�鷽��
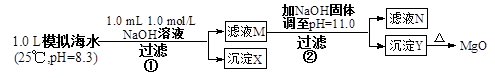
ģ�⺣ˮ�е�
����Ũ��(mol/L)
| Na��
| Mg2��
| Ca2��
| Cl�D
| 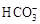
|
0.439
| 0.050
| 0.011
| 0.560
| 0.001
|
ע����Һ��ij�����ӵ�Ũ��С��1.0��10��5 mol/L������Ϊ�����Ӳ����ڣ�
ʵ������У�������Һ������䡣
��֪��Ksp(CaCO3)��4.96��10��9��Ksp(MgCO3)��6.82��10��6��
Ksp[Ca(OH)2]��4.68��10��6��Ksp[Mg(OH)2]��5.61��10��12��
����˵����ȷ���ǣ�?��
A��������XΪCaCO3
B����ҺM�д���Mg2����������Ca2��
C����ҺN�д���Mg2����Ca2��?
D�������������Ϊ����4.2 g NaOH���壬������YΪCa(OH)2��Mg(OH)2�Ļ����