1、简答题 氯化铍是用于制有机铍化合物和金属铍的重要原料.
(1)Be原子的基态价电子排布式为______,其元素的第一电离能______B元素(填“>”或“<”或“=”),原因是______.
(2)已知BeCl2加热易升华,液态BeCl2不导电,则BeCl2晶体类型为______;?BeCl2中Be原子的杂化轨道类型是______.
(3)Kraus用阴离子树脂交换法提取一种组成元素为氯和铍的阴离子,该阴离子内铍原子最外层达到8电子稳定结构,则该阴离子内存在的微粒间的作用力是______,阴离子的结构式为______.
参考答案:(1)Be原子的电子排布式为1s22s2,Be原子的基态价电子排布式为2s2.Be的2s轨道为全充满,稳定状态,体系能量低,第一电离能高于同周期相邻元素.
故答案为:2s2;>;Be的2s轨道全充满,体系能量低.
(2)BeCl2加热易升华,液态BeCl2不导电,则BeCl2晶体类型为分子晶体;BeCl2中Be原子成2个Be-Cl,Be原子的杂化轨道数为2,故Be原子采取?sp?杂化方式.
故答案为:分子晶体;?sp.
(3)阴离子内铍原子最外层达到8电子稳定结构,离子为BeCl42-,Be原子与氯原子之间通过共价键与配位键达8电子稳定结构,结构式为.
故答案为:共价键、配位键;
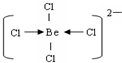
.
本题解析:
本题难度:一般
2、选择题 某原子核外共有n个电子层(n>3),则(n-1)层最多容纳的电子数为( )
A.8个
B.18个
C.32个
D.无法确定
参考答案:某原子核外共有n个电子层(n>3),则(n-1)层大于或等于第三电子层,为次外层,最多容纳的电子数为18.
故选:B.
本题解析:
本题难度:简单
3、填空题 按下面所要求的化学用语,表示出下列元素的原子(或离子)结构
(1)铁元素原子的电子排布式:__________;
(2)铬(原子序数24)元素的简写电子排布式(用“原子芯”表示内层):_________;
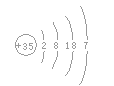
(3)溴元素的原子结构示意图:___________;
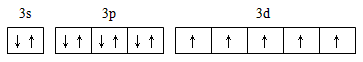
(4)Fe3+的最外层电子的轨道表示式:___________。
参考答案:(1)?1s22s22p63s23p63d64s2
(2)[Ne] 3s23p63d54s1
(3)
(4)
本题解析:
本题难度:一般
4、填空题 写出下列元素基态原子的电子排布式
(1)N ________________
(2)Ne ________________
(3)S ________________
(4)Ca ________________
(5)29Cu ________________
(6)32Ge________________
参考答案:(1)1s22s22p3
(2)1s22s22p6
(3)1s22s22p63s23p4
(4)1s22s22p63s23p64s2
(5)1s22s22p63s23p63d104s1
(6)1s22s22p63s23p63d104s24p2
本题解析:
本题难度:一般
5、选择题 某主族元素的原子的最外层电子数是次外层的a倍(a>1),则该原子核内质子数是( )
A.2a
B.a+2
C.2a+10
D.2a+2
参考答案:D
本题解析:
本题难度:简单