1、选择题 对于实验Ⅰ~Ⅳ的实验现象预测正确的是
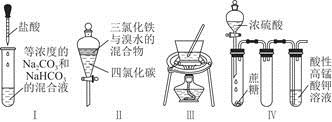
A.实验Ⅰ:逐滴滴加盐酸时,试管中立即产生大量气泡
B.实验Ⅱ:充分振荡后静置,下层溶液为橙红色,上层无色
C.实验Ⅲ:从饱和食盐水中提取NaCl晶体
D.装置Ⅳ:酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅直至褪去
参考答案:D
本题解析:实验Ⅰ,逐滴滴加盐酸时,首先发生反应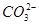 +H+===
+H+===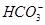 ,开始没有气泡,A项错误;实验Ⅱ,充分振荡并静置后,上层为氯化铁溶液的颜色,应为浅黄色,B项错误;实验Ⅲ,加热蒸发饱和食盐水应用蒸发皿而不是坩埚,C项错误;实验Ⅳ,将浓硫酸滴入蔗糖中发生反应生成SO2和CO2气体,SO2与酸性高锰酸钾溶液发生氧化还原反应,使之褪色,D项正确。
,开始没有气泡,A项错误;实验Ⅱ,充分振荡并静置后,上层为氯化铁溶液的颜色,应为浅黄色,B项错误;实验Ⅲ,加热蒸发饱和食盐水应用蒸发皿而不是坩埚,C项错误;实验Ⅳ,将浓硫酸滴入蔗糖中发生反应生成SO2和CO2气体,SO2与酸性高锰酸钾溶液发生氧化还原反应,使之褪色,D项正确。
本题难度:一般
2、选择题 将含等物质的量的氯化铵和碳酸氢钠混合溶液蒸干灼烧最终得到的固体是?
A.只有碳酸钠
B.只有氯化钠
C.一定是氯化钠和碳酸钠的混合物
D.碳酸铵
参考答案:B
本题解析:氯化铵灼烧分解生成氯化氢和氨气,碳酸氢钠受热分解生成碳酸钠,二氧化碳,水,由于混合在一起,氯化氢又和碳酸钠反应生成氯化钠,最终只剩余氯化钠。?故选B。
本题难度:一般
3、选择题 下列反应与Na2O2+SO2→Na2SO4相比较,Na2O2的作用相同的是
A.2Na2O2+2CO2→2Na2CO3+O2
B.2Na2O2+2SO3→2Na2SO4+O2
C.2Na2O2+H2SO4→Na2SO4+H2O2
D.3Na2O2+Cr2O3→2Na2CrO4+Na2O
参考答案:D
本题解析:反应Na2O2+SO2→Na2SO4中SO2是还原剂,过氧化钠是氧化剂,则A、反应2Na2O2+2CO2→2Na2CO3+O2中过氧化钠既是氧化剂,也还原剂,A不正确;B、反应2Na2O2+2SO3→2Na2SO4+O2中过氧化钠既是氧化剂,也还原剂,B不正确;C、反应2Na2O2+H2SO4→Na2SO4+H2O2中元素的化合价均没有发生变化,不是氧化还原反应,C不正确;D、反应3Na2O2+Cr2O3→2Na2CrO4+Na2O中,过氧化钠是氧化剂,D正确,答案选D。
本题难度:简单
4、选择题 下列各组物质中,反应后生成碱和氧气的是(?)。
A . Na和H2O? B. Na2O和H2O? C. CaO和H2O? D. Na2O2和H2O
. Na和H2O? B. Na2O和H2O? C. CaO和H2O? D. Na2O2和H2O
参考答案:D
本题解析:略
本题难度:简单
5、填空题 (6分)
(1)Na与水反应的化学方程式是:?。
(2) 由Al与Fe2O3组成的铝热剂常用于焊接铁轨。Al与Fe2O3混合强热反应的的化学方程式为:?。
参考答案:(1)2Na + 2H2O ="==" 2NaOH + H2↑(2)2Al + Fe2O3高温 2Fe + Al2O3
本题解析:(1)2Na + 2H2O ="2NaOH" + H2↑
(2)2Al + Fe2O3高温 2Fe + Al2O3
本题难度:简单