1、选择题 下列关于 Na2CO3和NaHCO3性质比较中正确的是(?)
A.热稳定性:Na2CO3< NaHCO3
B.常温时水溶解性::Na2CO3<NaHCO3
C.等质量时与盐酸反应产生CO2的质量:Na2CO3<NaHCO3
D.与同浓度稀盐酸反应快慢:NaHCO3<Na2CO3
参考答案:C
本题解析:碳酸氢钠加热发生分解,碳酸钠加热不分解,A错误;常温时碳酸氢钠溶解度小于碳酸钠,B错误;等质量碳酸钠与碳酸氢钠与足量盐酸反应生成二氧化碳碳酸氢钠多,C正确;与同浓度盐酸反应时碳酸氢钠比碳酸钠快。
点评:向碳酸钠溶液中滴加碳酸钠,反应依次为:CO32-+H+=HCO3-、HCO3-+H+=H2O+CO2↑。
本题难度:一般
2、选择题 下列关于Na2CO3和NaHCO3的说法中,错误的是(? )
A.可以用澄清的石灰水鉴别Na2CO3溶液和NaHCO3溶液
B.等物质的量的Na2CO3和NaHCO3,与足量盐酸反应生成CO2也相同
C.NaHCO3与NaOH固体加热后,可生成Na2CO3
D.两溶液的焰色均为黄色
参考答案:A
本题解析:Na2CO3和NaHCO3与Ca(OH)2反应均生成CaCO3白色沉淀,A项错误。由化学方程式或碳的守恒可知B项正确。NaHCO3酸式盐,在溶液中与NaOH溶液反应,或NaHCO3和NaOH两固体加热反应,均生成Na2CO3和H2O,C项正确。钠的焰色为黄色,D项正确。
本题难度:一般
3、实验题 某未知溶液X中可能含有K+、Fe2+、NH4+、Cl-。检验其中是否含有K+,通常有如下两套实验方案。
方案一:焰色反应法
用洁净的玻璃棒蘸取未知液X置于酒精灯外焰上灼烧,观察到火焰呈黄色,则证明其中不含K+。对上述实验过程中的错误和疏漏之处加以纠正、补充:?、
?。
方案二:亚硝酸钴钠法
在CH3COOH酸化的溶液中,K+与亚硝酸钴钠[Na3Co(NO2)6]反应生成黄色沉淀[K2NaCo(NO2)6],该原理可用于K+的检验。注意:NH4+也能与Na3Co(NO2)6生成黄色沉淀,会干扰K+离子的检验。请你利用上述反应原理设计一个实验方案,检验未知溶液X中是否含有K+。
?
?。
参考答案:方案一:应使用铂丝或无锈铁丝蘸取溶液?应透过蓝色钴玻璃观察
方案二:向未知溶液X中加入稍过量的NaOH溶液并加热;静置、冷却后取上层清液
少许;用醋酸酸化后再加入亚硝酸钴钠,观察是否有黄色沉淀生成。(或者取未知液X蒸干并灼烧,将所得固体溶于水,过滤;取少量滤液,用醋酸酸化后再加入亚硝酸钴钠,观察是否有黄色沉淀生成。)
本题解析:方案二中的关键问题是题中所给信息: NH4+也能与Na3Co(NO2)6生成黄色沉
淀,会干扰K+离子的检验。那首先要除去NH4+,加入NaOH溶液,除去NH4+同时会生成Fe(OH)2等沉淀,因此要过滤。由题所知加酸中和过量的氢氧化钠,要用醋酸,不宜使用HNO3。
本题难度:简单
4、实验题 为了探究SO2与Na2O2的反应是否类似于CO2与Na2O2的反应,甲同学设计了如图所示的实验装置,回答下列问题:

(1)移开棉花,将带火星的木条放在C试管口,未见木条复燃,甲同学因此认为SO2与Na2O2的反应不同于CO2。请按甲同学的观点写出反应的化学方程式?。
(2)乙同学认为无论反应原理如何,最终都有O2产生,乙同学的理由是?。按照乙同学的观点,该装置需做的改进是?
?。
(3)假设Na2O2完全反应,反应后B装置中固体生成物可能是:①Na2SO3;②Na2SO4;③Na2SO3和Na2SO4。
请设计实验方案检验,写出实验步骤以及预期现象和结论,完成下表:
限选试剂:2 mol・L-1 HCl溶液,1 mol・L-1 HNO3溶液,1 mol・L-1 BaCl溶液,1 mol・L-1 Ba(NO3)2溶液,0.01 mol・L-1 KMnO4酸性溶液。
实验步骤
| 预期现象和结论
|
步骤1:取B中的少量固体样品于试管中,滴加足量蒸馏水,溶解,然后取少量待测液分别置于Ⅰ、Ⅱ试管中
| 固体完全溶解
|
步骤2:往Ⅰ试管中加入?,再滴加?
| ?,
|
则证明生成物中含Na2SO4
| ?
|
步骤3:往Ⅱ试管中?
| ?
|
?
| 若?,
|
则证明生成物中有Na2SO3;若
| ?
|
?
| ?
|
则说明生成物中没有Na2SO3。
| ?
|
?
(4)生成物中亚硫酸钠含量的测定:
①取a g生成物配制成100 mL溶液,取10.00 mL该溶液于锥形瓶中,加入几滴淀粉溶液作指示剂,用0.010 0 mol・L-1碘水进行滴定,滴定终点现象为?。记录数据,重复滴定2次,平均消耗碘水20.00 mL。
②计算:生成物中亚硫酸钠的质量分数为?。
参考答案:(1)SO2+Na2O2=Na2SO4
(2)A中生成的SO2气体中含有水蒸气
在A和B之间连接一个装有浓硫酸的洗气瓶(或其他合适的干燥装置)
(3)
步骤2:往Ⅰ试管中加入足量的1_mol・L-1盐酸,再滴加1_mol・L-1_BaCl2溶液
有白色沉淀生成,则证明生成物中含Na2SO4
步骤3:往Ⅱ试管中加入2~3滴0.01_mol・L-1_KMnO4酸性溶液,振荡
若KMnO4溶液紫红色褪去,则证明生成物中有Na2SO3;
若KMnO4溶液紫红色不褪去,则说明生成物中没有Na2SO3
?
(4)①溶液出现蓝色,且半分钟内不褪色
②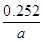 ×100%
×100%
本题解析:(1)~(2)实验的原理可解读为:将反应后所得气体通过足量NaOH溶液除去过量SO2后,该气体不能使带火星木条复燃说明反应中没有O2生成;而乙同学的观点是考虑到水蒸气的影响,故需要设计实验将气体干燥后再用带火星木条检验是否为O2。(3)根据假设中的三种情况,设计实验的目的就是检验所得固体中是否含有SO42-和SO32-,SO42-的检验可利用BaCl2和稀盐酸;SO32-的检验可根据其还原性,利用溶液是否能使酸性高锰酸钾溶液褪色来进行。(4)①滴定过程中发生的反应为H2O+SO32-+I2=2I-+SO42-+2H+,故滴定终点时的现象为溶液出现蓝色,且半分钟内不褪色。②由①中离子方程式可得关系式Na2SO3~I2,故生成物中亚硫酸钠的质量分数为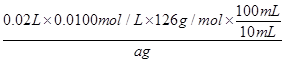 ×100%=
×100%=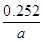 ×100%。
×100%。
本题难度:困难
5、选择题 下列叙述中正确的是
[? ]
A.Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
B.Na2O能继续被氧化成Na2O2
C.Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成O2
D.Na2 O2只有还原性
参考答案:B
本题解析:
本题难度:简单