1���ƶ��� X��һ���������ǽ������ϣ�������ĥ����ʴ�������ȳ���ԡ��й�������������
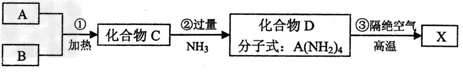
Ϊ��ȷ��C����ɣ�ijͬѧ���������µ�̽�����̡���֪F��G����������ˮ��ϡ����İ�ɫ������I�������ά��
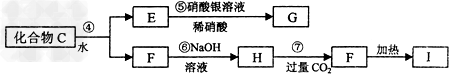
��Ҫ��ش��������⣺
��1��C�Ļ�ѧʽΪ___________��X�Ļ�ѧʽΪ_____________?��
��2��д�����з���ʽ��Ӧ�ڵĻ�ѧ����ʽ________________����Ӧ�ߵ����ӷ���ʽ____________________________?��
�ο��𰸣���1��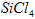 ��
��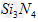
��2��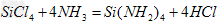 ��
��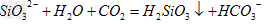
���������
�����Ѷȣ�һ��
2������� ��֪AΪ��ѧ��ѧ�е�һ���Σ�B��CΪ�ճ������г����Ľ�����ͨ��������D��GΪ��ɫ��ζ���壮��֪�ö��Ե缫���A��Һһ��ʱ�����ֻ��C��D��E��ϡ��Һ��������֮���ת����ϵ��ͼ�����ַ�Ӧ��������ȥ����
��ش��������⣺
��1��A�Ļ�ѧʽΪ______��
��2��A��Һ��Na2O2��Ӧ���ܻ�ѧ����ʽΪ______��
��3��E��ϡ��Һ��F��Һ��Ӧ�����ӷ���ʽΪ______��
��4�����100mL��A����Һһ��ʱ��Ͽ���·��ȡ���缫��������õ�������D�ڱ�״���µ����Ϊ5.6mL���������Һ��pHΪ______����������Һ������䣩
��5������100mL��A����Һ�м���10g��������B�ķ�ĩ����ֽ�����ˣ���ɵ�10.16g����C������Һ�����ʵ����ʵ���Ũ��Ϊ______����������Һ������䣩
�ο��𰸣���1�����A��Һʱ������������C������һ������D��ӦΪ��⺬��������Һ�������������������ý�������CӦΪͭ��DΪ������E��Һ����C��������������ԭ��Ӧ����E��Һ��F��ҺҲ�ܷ�Ӧ������ɫ��ζ����G��˵��E��Һ����ǿ�����ԣ�ӦΪ���ᣬ��AΪ���ᣬCΪͭ��DΪ������GΪNO��F�����ᷴӦ����NO��˵���Һ��н���BԪ�أ�˵��F��Һ���л�ԭ�ԣ�ӦΪFe��NO3��2��Һ��BΪFe��HΪFe��NO3��3���ʴ�Ϊ��Cu��NO3��2��
��2��Na2O2��ˮ���뵽Cu��NO3��2��Һ�з�Ӧ����NaOH��������NaOH��Cu��NO3��2��Ӧ������ɫ����2Cu��OH��2���ʴ�Ϊ��2Na2O2+2Cu��NO3��2+2H2O=2Cu��OH��2��+4NaNO3+O2����
��3���������ǿ�����ԣ�Fe2+���л�ԭ�ԣ����߷���������ԭ��Ӧ���ʴ�Ϊ��3Fe2++NO3-+4H+�T3Fe3++NO��+2H2O��
��4�����ݵ������ͭ�ĵ缫����ʽ��
2Cu��NO3��2+2H2O?���?.?2Cu+O2��+4HNO3
? ? 22.4L? 4mol
? 5.6��10-3L? n
��n=4��mol��5.6��10-322.4L?L=1��10-3mol
����c��H+��=1��10-3mol0.1L=0.01mol����PH=2���ʴ�Ϊ��2��
��5������A��Һ�м����������B����Ӧ�Ļ�ѧ����ʽΪ��Fe+Cu��NO3��2�TFe��NO3��2+Cu�����ݲ��������㣺
Fe+Cu��NO3��2�TFe��NO3��2+Cu��m
? 1mol?8g
? n? 10.16g-10g=0.16g
n=0.168=0.02mol��������Һ��Ũ��Ϊ��0.02mol0.1L=0.2mol/L���ʴ�Ϊ��0.2?mol/L��
���������
�����Ѷȣ���
3������� ��һ�������¿�ʵ����ͼ��ʾ����֮����ת�䣺

(1)��������Ʋ⣬����д�������ʵĻ�ѧʽ��
A��______��B��______��D��______��G��______��
(2)��Ҫ˵��A��ת��ΪB��C��ԭ��д���йط�Ӧ�Ļ�ѧ����ʽ��
___________________________________________________
(3)д��E������A��Һ��Ӧ�����ӷ�Ӧ����ʽ��______
�ο��𰸣�(1)A��FeCl3��6H2O��B��HCl��D��FeS��G��Fe
(2)��FeCl3��6H2O����ˮ�⣬HCl�ӷ���Fe(OH)3���ֽ�����Fe2O3
2FeCl3��6H2O Fe2O3+6HCl��+3H2O
Fe2O3+6HCl��+3H2O
(3)H2S+2Fe3+=2Fe2++S��+2H+
�����������ɫ����B����������Һ������ɫ������˵��B�к�����Ԫ�أ�C����ɫ���弴Fe2O3����B���ɺ�A����Һ�����뱽�ӻ�Ͽɳ���ɫ��˵��AΪFeCl3��6H2O��BΪHCl
E�г�������ζ�����壬��ΪH2S����A��ӦΪ��H2S+2Fe3+=2Fe2++S��+2H+����FΪFeCl2��HΪ��
FeCl3��G��������F��FeCl2������G����2FeCl3��Fe=3FeCl2������������D��S��Fe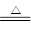 FeS
FeS
B��D�ķ�ӦΪ��FeS��2HCl=FeCl2��H2S��
��2��FeCl3��6H2O���ȴٽ�ˮ�⣬����HCl�ӷ���ת��ΪFe(OH)3������ˮ����Fe2O3������2FeCl3��6H2O Fe2O3+6HCl��+3H2O
Fe2O3+6HCl��+3H2O
�����Ѷȣ�һ��
4���ƶ��� A~F������ת����ϵ����Ӧ���ڸ����½��У���ҪʱҪ�ô���������֪A�dz����������ʣ�B�ڳ�����ΪҺ̬��E������N2�ĵ�������ͬ��

(1)��֪��Ӧ����A��B������Ӧÿ����1molDʱ�ų�QkJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ��________��
(2)д����Ӧ�۵Ļ�ѧ����ʽ��_______________��
(3)д��һ�����û���Ӧ��F��Ϊ�������Ļ�ѧ����ʽ��______________��
(4)д��һ���ܽ�B�������������Ļ�ѧʽ__________________��
�ο��𰸣�(1)3Fe(s) +4H2O(g) Fe3O4(s)+4H2(g) ��H=-4QkJ/mol
Fe3O4(s)+4H2(g) ��H=-4QkJ/mol
(2)CO+H2O(g) CO2+H2
CO2+H2
(3)2Mg+CO2 C +2MgO
C +2MgO
(4) F2
���������
�����Ѷȣ�һ��
5������� �ס��ҡ�����������֮��������ת����ϵ����
������
��1�����ͱ����Dz�����ˮ�İ�ɫ�������ʣ�������������������������������Һ�������______������______���ѧʽ����д����������ת�������ӷ���ʽ��______��
��2��������Һ�м���KSCN��Һ����Ѫ��ɫ���֣������______������______���ѧʽ����д�������ҡ�ת�������ӷ���ʽ��______��
�ο��𰸣���1���ͱ����Dz�����ˮ�İ�ɫ�������ʣ�������������������������������Һ˵�����������ʣ����ת����ϵ�жϣ����������������ȷֽ�õ���Ϊ������������������������Al2O3�����ڼ���ǺͰ�ˮ��Ӧ���ɵ�������������Al��OH��3��������������ǿ��ǿ���������������ҵ����ķ�ӦΪ��������һˮ�ϰ���Ӧ������������������泥����ӷ���ʽΪ��Al3++3NH3?H2O=Al��OH��3��+3NH4+��
�ʴ�Ϊ��Al2O3��Al��OH��3��Al3++3NH3?H2O=Al��OH��3��+3NH4+��
��2������Һ�м���KSCN��Һ����Ѫ��ɫ����֤�����������ӣ���Ϊ����������Ȼ����ɼף�˵�����������������������Fe2O3����Ϊ�������������ҷ�Ӧ�ķ�Ӧ�����ӷ���ʽΪ��Fe2O3+6H+=2Fe3++3H2O���ʴ�Ϊ��Fe2O3��Fe��OH��3��Fe2O3+6H+=2Fe3++3H2O��
���������
�����Ѷȣ�һ��