1、选择题 下列物质的制取,实验操作正确的是
A.将CuCl2溶液置于蒸发皿中加热蒸干,可制取无水CuCl2固体
B.将NH4HCO3饱和溶液置于蒸发皿中加热蒸于,可制取NH4HCO3固体
C.向FeCl3饱和溶液中缓慢滴入过量氨水加热,可制取Fe(OH)3胶体
D.向电石中缓慢滴入饱和食盐水,可制取C2H2
参考答案:D
本题解析: A、氯化铜溶液中水解生成氢氧化铜和盐酸,蒸干溶液得到氢氧化铜,不能制备氯化铜,故A错误;B、碳酸氢铵受热分解,将NH4HCO3饱和溶液在蒸发皿中加热蒸干不能得到碳酸氢铵,故B错误;C、氯化铁溶液中加入过量氨水反应生成氢氧化铁沉淀,不能生成氢氧化铁胶体,故C错误;D、饱和食盐水和电石反应生成乙炔气体,减缓反应进行程度,可以制取乙炔,故D正确;故选D。
本题难度:一般
2、选择题 下列溶液中微粒的物质的量浓度关系一定正确的是( )
A.某二元弱酸的酸式盐NaHA溶液中:c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-)
B.0.2 mol/L NH4Cl溶液和 0.1 mol/L NaOH溶液等体积混合:c(NH4+)>c(Cl-)>c(Na+)>c(OH-)>c(H+)
C.pH=2的HA溶液与pH=12的MOH溶液等体积混合:c(M+)=c(A-)>c(OH-)=c(H+)
D.25℃时,pH=8的CH3COONa稀溶液中:c(CH3COOH)=9.9×10-7 mol/L
参考答案:D
本题解析:A项溶液中电荷不守恒,应为:c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)。B项溶液中,反应后生成等物质的量的NH4Cl、NaCl和NH3・H2O,c(Cl-)>c(NH4+)。C项中酸、碱的强弱不确定,反应后所得的溶液可能显酸性、中性或碱性。D项溶液中,电荷守恒式为:c(Na+)+c(H+)=c(CH3COO-)+c(OH-);物料守恒式为:c(Na+)=c(CH3COO-)+c(CH3COOH),则c(CH3COOH)=c(OH-)-c(H+)=(10-6-10-8) mol/L=9.9×10-7 mol/L。
本题难度:一般
3、选择题 在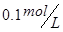
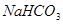 溶液中,下列关系中不正确的是
溶液中,下列关系中不正确的是
A.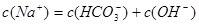
B.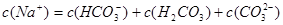
C.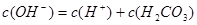 -c(CO32-)
-c(CO32-)
D.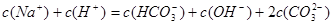
参考答案:A
本题解析:略
本题难度:简单
4、选择题 下列物质溶解于水时,电离出的阴离子能使水的电离平衡向右移动的是(?)
A.Na2SO4
B.CH3COONa
C.NH4Cl
D.HClO
参考答案:B
本题解析:A 对水的电离平衡无影响
B 醋酸根离子会水解,促进水的电离
C 铵根离子会水解,促进水的电离,但是铵根离子是阳离子,不是阴离子
D HclO会抑制水的电离
故选B
本题难度:一般
5、填空题 回答下列有关Na2S溶液的问题。
(1)Na2S溶液盛装在带橡胶塞的试剂瓶中,仔细闻有臭鸡蛋气味,请用离子方程式解释:
?,?。
(2)将Na2S溶液加入AlCl3溶液中,有白色沉淀和臭鸡蛋气味的气体生成,发生的离子反应为:
?。
(3)将Na2S溶液加入AgCl的浊液中,生成的黑色沉淀是?(写化学式)。
参考答案:(1)S 2-+ H2O HS- +OH-,? HS-+ H2O
HS- +OH-,? HS-+ H2O H2S +OH-
H2S +OH-
(2)2Al 3+ + 3S 2-+6 H2O = 3H2S↑+ 2Al(OH)3↓
(3)Ag2S
本题解析:(1)多元弱酸根离子要分步水解,以第一步为主
(2)Al 3+与S 2-水解生成Al(OH)3沉淀
(3)S 2-与 结合成Ag2S
结合成Ag2S
本题难度:一般