1、选择题 两种微粒的质子数.电子数均相等,则它们可能是:①同位素;②不同的分子;③不同的离子;④同一元素的不同离子。则上述说法正确的是
[? ]
A.①②③④
B.①③④
C.③④
D.①②③
参考答案:D
本题解析:
本题难度:一般
2、选择题 下列说法中错误的是
[? ]
A.原子及其离子的核外电子层数等于该元素所在的周期数
B.除氦外的稀有气体原子的最外层电子数都是8
C.元素周期表中ⅢA族元素不都是金属元素
D.同一元素的各种同位素的化学性质均相同
参考答案:A
本题解析:
本题难度:简单
3、选择题 下表为元素周期表前4周期的一部分,且X、Y、Z、R和W为主族元素。下列说法正确的是
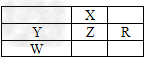
[? ]
A.五种元素一定都是非金属元素
B.五种元素的原子最外层电子数一定大于2
C.Z的氧化物与X单质在任何条件下都不会发生置换反应
D.R的最外层电子数一定为5
参考答案:B
本题解析:
本题难度:简单
4、选择题 下列叙述正确的是
①热稳定性:H2O>HF>H2S
②熔点:Al>Na>K
③ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
④元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑤多电子原子中,在离核较近的区域内运动的电子能量较高
⑥已知2H2(g)+O2(g)=2H2O(l)△H= -571kJ・mol-1 则氢气的燃烧热为-285.5kJ・mol-1
⑦因为常温下白磷可自燃,而氮气须在放电时才与氧气反应,所以非金属性:P>N
A.只有②④⑥
B.只有①⑤⑥
C.只有②③④
D.只有③⑤⑦
参考答案:A
本题解析:①错,氢化物的稳定性是比较对应元素的非金属性强弱,非金属性越强,氢化物越稳定;②正确;③错,ⅠA、ⅡA族元素的阳离子与上周期稀有气体元素的原子具有相同的核外电子排布;④正确;⑤错,多电子原子中,在离核较近的区域内运动的电子能量较低;⑥正确;⑦错,非金属性的强弱与反应条件无关;
本题难度:简单
5、选择题 各组性质比较的表示中,正确的是( )
A.酸性:HI<HBr<HCl<HF
B.稳定性:HF<HCl<HBr<HI
C.氧化性:F2<Cl2<Br2<I2
D.沸点:F2<Cl2<Br2<I2
参考答案:A、气态氢化物稳定性为HI<HBr<HCl<HF,则酸性为HI>HBr>HCl>HF,故A错误;
B、因非金属性F>Cl>Br>I,则稳定性为HF>HCl>HBr>HI,故B错误;
C、非金属性越强,单质的氧化性越强,非金属性F>Cl>Br>I,则氧化性为F2>Cl2>Br2>I2,故C错误;
D、卤族元素的单质,相对分子质量越小,熔沸点越低,则沸点为F2<Cl2<Br2<I2,故D正确;
故选D.
本题解析:
本题难度:简单