1、推断题 A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含一种金属元素。A和D最外层电子数相 同;B、C和E在周期表中相邻,且C、E同主族。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的化合物甲和乙(相对分子质量甲<乙)。
请回答下列问题:
(1)甲的电子式为___________;写出乙的一种用途____________。
(2)用某种废弃的金属易拉罐和碳棒作电极,以A、C、D 组成的化合物溶液为电解质溶液,构成原电池,写出负极的电极反应式________________。
(3)向A、B、C三种元素组成的某盐溶液中滴加AgNO3溶液生成白色沉淀,该反应的化学方程式为________________。反应后的溶液中浓度最大的离子为__________(写离子符号)。
(4)写出C和D形成的化合物与EC2发生氧化还原反应的化学方程式,并标出电子转移的方向和数目
___________________。
参考答案:(1) ;杀菌、消毒
;杀菌、消毒
(2)Al+4OH--3e-=AlO2-+2H2O?
(3)NH4NO2+AgNO3=AgNO2↓+NH4NO3;NO3- (4)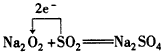
本题解析:
本题难度:一般
2、选择题 下列递变规律正确的是
A.热稳定性:HCl >HF >H2O
B.沸点:金刚石>冰>干冰
C.碱性:NaOH >Mg(OH)2>Ca(OH)2
D.元素的最高正化合价:F>S>C
参考答案:B
本题解析:非金属性越强,氢化物的稳定性越强,A不正确,应该是HF >H2O> HCl 。金刚石是原子晶体,冰和干冰是分子晶体,水中含有氢键,所以沸点高于干冰的,B正确。金属性越强,最高价氧化物的水化物的碱性越强,C中应该是Ca(OH)2>NaOH >Mg(OH)2。F是最强的非金属,没有正价,D不正确,所以答案选B。
本题难度:简单
3、填空题
在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 molXY2含有54 mol电子。
(1)该融雪剂的化学式是_________;X与氢元素形成的化合物的电子式是_________。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是_________;D与E能形成一种非极性分子,该分子的结构式为_________;D所在族元素的氢化物中,沸点最低的是_________。
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价健;W与Z能形成一种新型无机非金属材料,其化学式是_________。
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为__________________。
参考答案:(1)CaCl2;
(2)S=C=S;H2S
(3)Si3N4
(4)2F2+2OH-=2F-+OF2+H2O
本题解析:
本题难度:一般
4、选择题 下列各表分别是元素周期表的一部分,表中的数字表示元素的原子序数,各表中数字所表示的元素在周期表中的位置与周期表的结构相符的是( )
A.
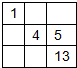
B.
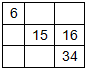
C.
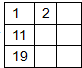
D.
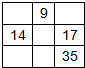
参考答案:A、4和5,12和13间有10个空列为7个副族和1个Ⅷ族,故A错误;
B、中列为7、15、33,中行为14、15、16,符合位置关系,故B正确;
C、1号和11号元素之间相隔一个周期,第一列应为1、3、11、19,2号元素与1号元素之间相隔16列,故C错误;
D、14号元素与17号元素之间相隔2列,9号元素与17号、35号元素,处于同列,故D错误.
故选:B.
本题解析:
本题难度:一般
5、简答题 下表是元素周期表的一部分.
族
周期 | | II?A | | IV?A | | | VII?A
1
① |
2
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
(11)
|
(1)表中所列元素中,最稳定的气态氢化物的化学式______,原子半径最小的元素的元素符号是______.
(2)某元素原子的核外M层电子数是元素②最外层电子数的1/2,则该元素的元素符号是______,其元素原子结构示意图为______.
(3)某元素是组成蛋白质的重要成分,蛋白质又是生命的存在形式,因此此元素被称为“生命元素”,此元素的名称为______,其单质的电子式为______,用化学方程式表示其单质的一种重要的工业用途:______.
(4)④与⑥形成原子个数之比为1:1的化合物的电子式为______,用电子式表示⑤和⑩形成化合物的过程______
(5)写出下列化学方程式
⑤的单质通入⑥和⑨形成化合物的水溶液中______
⑨的单质通入⑥和(11)形成化合物的水溶液中______.
参考答案:根据元素在周期表中的分布,可以推知①是H,②是C,③是N,④是O,⑤是F,⑥是Na,⑦是Al,⑧是S,⑨是Cl,⑩是Ca,(11)是Br.
(1)在周期表中,从左到右的电子能力逐渐增强,从上到下得电子能力逐渐减弱,得电子能力最强的是F,原子半径最小的是H,所以HF是最稳定的氢化物,故答案为:HF;H;
(2)原子的核外M层电子数是C元素最外层电子数的1/2即核外电子排布分别是2、8、2,应为Mg,原子结构示意图为:
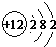
,故答案为:Mg;
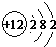
;
(3)氮元素被称为“生命元素”,氮气中含有氮氮三键,电子式为:

,在工业生可以用氮气和氢气来合成氨,即?N2+3H2高温高压
本题解析:
本题难度:一般