1、推断题 A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。A原子核内无中子;A和E、D和F分别同主族,且B与D最外层电子数之比为2:3。试回答下列问题:
(1)E元素在周期表中的位置是_____________;
(2)已知101KPa时,A单质的燃烧热为285.8kJ/mol,请写出A单质完全燃烧生成液态水时的热化学方程式:___________________;
(3)E单质在足量D单质中燃烧生成的化合物的电子式是_____________;
(4)化合物X、Y均由A、D、E、F四种元素组成。
①X、Y均属于________化合物(填“离子”或“共价”):
②X与Y的水溶液相混合发生反应的离子方程式为__________________;
(5)化合物E2F的水溶液中滴入双氧水和稀硫酸,加热,有单质生成。其离子反应方程式为:__________________________。
2、选择题 下列叙述中正确的是
[? ]
A.SiO2是酸性氧化物可以和水反应生成硅酸
B.HF很稳定,是因为HF分子间存在着氢键
C.Na?和Cs?属于第IA?族元素,Cs?失电子能力比Na的强
D.P?和As属于第VA?族元素,H3PO4酸性比H3AsO4的弱
3、填空题 在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1mol XY2含有54 mol电子。
(1)该融雪剂的化学式是_______________;X与氢元素形成的化合物的电子式是______________。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是
_______________;D与E能形成一种非极性分子,该分子的结构式为_______________;D所在族元素的氢化物中,沸点最低的是_______________。
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价健;W与Z能形成一种新型无机非金属材料,其化学式是_______________。
4、选择题 下列排列顺序正确的是
[? ]
①热稳定性:HF>H2O>NH3 ②离子半径:Na+>Mg2+>F-?③酸性:盐酸>碳酸>醋酸?④结合质子能力:OH->CO32->HCO3- ?
A.①③?
B.②④?
C.①④?
D.②③
5、推断题 短周期元素的A、B、C在元素周期表中的位置如图所示,已知A、C两种元素的原子核外电子数之和等于B的质子数。
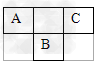
据此填空: ?
(1)B的元素符号为________,原子结构示意图为 在周期表中位置__________;
(2)A的氢化物电子式为________,C单质的电子式___________ C的单质与水反应的化学方程式为______________。