1、填空题 (10分)
1)在Fe3O4 +4CO 3Fe+4CO2的反应中,?是氧化剂,?是还原剂,?元素被氧化,?元素被还原。
3Fe+4CO2的反应中,?是氧化剂,?是还原剂,?元素被氧化,?元素被还原。
2)配平下列化学方程式并用单线桥法分析下列氧化还原反应中电子转移的方向和数目,
?Cu +?HNO3(浓)?― ?Cu(NO3)2 + ?NO2↑ +?H2O
浓硝酸表现出来的性质是_______________(填写编号)。?
①还原性? ②酸性? ③氧化性? ?
参考答案:
本题解析:略
本题难度:一般
2、选择题 下列反应中,SO2被还原的是(?)
A.SO2+2NaOH====Na2SO3
B.SO2+Cl2+2H2O====H2SO4+2HCl
C.SO2+2H2S====3S+2H2O
D.SO2+NO2====SO3+NO
参考答案:C
本题解析:SO2被还原,则硫的化合价将降低,生成单质硫,故选C。
本题难度:简单
3、填空题 一个体重50 kg的健康人含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
(1)经常进行Fe2+与Fe3+的转化,可表示为Fe2+?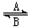 ?Fe3+。在过程A中,Fe2+作?剂。
?Fe3+。在过程A中,Fe2+作?剂。
(2)维生素C可使食物中的Fe3+转化为Fe2+,维生素C在这个反应中具有?性。
(3)某同学要检验Fe3+,向溶液中加入 ?(写化学式)溶液变成红色。要除去FeCl3溶液中少量的氯化亚铁,可行的办法是??(填字母)。
a.加入铜粉? b.加入铁粉? c.通入氯气? d.加入NaOH溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式??。
(4)电子工业常用30%的FeCl3 溶液腐蚀铜箔,制造印刷线路板,写出FeCl3 与金属铜反应的离子方程式 ?。
(5)使用过的腐蚀液会失效,但可以回收利用,某兴趣小组为了从使用过的腐蚀液中回收铜,应使用的试剂是??(填字母)
a.铜粉? b.氯气? c.铁粉? d.KSCN溶液
参考答案:(8分)(1)还原(1分);?(2)还原(1分);
(3)KSCN (1分)? c (1分)
2Fe2++Cl2==2Fe3++2Cl?(1分)
(4)2Fe3++Cu2+==2Fe2++Cu2+(1分)
(5)c (2分)
本题解析:(1)在A中铁元素的化合价由+2价升高到+3价,铁元素的化合价升高,则A中Fe2+做还原剂。
(2)由信息维生素C可使食物中的三价铁离子还原成二价铁离子,该反应中铁元素的化合价降低,则维生素C中某元素的化合价升高,即维生素C为还原剂,体现还原性。
(3)Fe3+和KSCN溶液发生特征反应,反应后溶液呈红色。氯化亚铁被强化剂氧化呈氯化铁,故选c。离子方程式为2Fe2++Cl2==2Fe3++2Cl?。
(4)FeCl3 与金属铜发生氧化还原反应,铜溶解,反应的离子方程式为2Fe3++Cu2+==2Fe2++Cu2+。
(5)铁的活泼性大于铜的活泼性,置换出铜一般用铁,故选c。
点评:本题属于信息习题,考查氧化还原反应中氧化剂、还原剂及氧化性、还原性,明确元素的化合价变化来分析是解答本题的关键,难度中等。
本题难度:一般
4、选择题 实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4 + 16HCl(浓)="=" 2KCl + 2MnCl2 + 5Cl2 ↑ + 8H2O。下列叙述错误的是(?)
A.氧化剂是KMnO4
B.反应过程中,Cl元素化合价升高,HCl被氧化
C.当有0.10 mol电子发生转移时,生成的氯气的体积为2.24 L(标准状况)
D.当生成2.24L(标准状况)氯气时,反应消耗HCl的物质的量为0.32mol
参考答案:C
本题解析:反应的双线桥如下:

C.转移的电子和生成的氯气的体积之比为:2:1,当有0.10 mol电子发生转移时,生成的氯气的体积为1.12L。
点评:本题把氧化还原反应和氯气的制取结合在一起考查学生,难度较大,但是抓住电子转移的本质,本题也可准确解答。
本题难度:一般
5、选择题 近日来,“巨能钙”事件沸沸扬扬,原因在于部分巨能钙被检出含有双氧水,而双氧水有致癌性,可加速人体衰老。因此卫生部已开始加紧调查“巨能钙”事件。下列有关说法错误的是(?)
A.双氧水是绿色氧化剂,可作医疗消毒剂,说明H2O2对人体无害
B.H2O2、Na2O2中都存在非极性共价键
C.H2O2既有氧化性,又有还原性,与KMnO4反应时表现H2O2的还原性
D.H2O2做漂白剂是利用其氧化性,漂白原理与HClO类似,和SO2不同
参考答案:A
本题解析:双氧水有致癌性,对人体有害,选项A是不正确,其余选项都是正确的,答案选A。
本题难度:一般