1、选择题 能正确表示下列反应的离子方程式是( )
A.向KHSO4溶液中加入Ba(OH)2溶液至恰好沉淀完全:Ba2++OH-+H++SO42-=BaSO4↓+H2O
B.铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑
C.碳酸钙与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O
D.硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓
参考答案:A.KHSO4溶液中加入Ba(OH)2溶液至恰好沉淀完全离子方程式:Ba2++OH-+H++SO42-=BaSO4↓+H2O,故A正确;
B.铁跟稀硫酸反应的离子反应为Fe+2H+═Fe2++H2↑,故B错误;
C.醋酸是弱酸,在离子方程式中不能拆成离子,应该为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故C错误;
D.硫酸铜溶液和氢氧化钡溶液反应生成Cu(OH)2和BaSO4,反应的离子方程式为Cu2++2OH-+SO42-+Ba2+═BaSO4↓+Cu(OH)2↓,故D错误.
故选A.
本题解析:
本题难度:一般
2、选择题 下列离子方程式书写正确的是(?)
A.铜溶于浓硝酸:Cu+4HNO3(浓) Cu2++2NO2↑+2H2O
Cu2++2NO2↑+2H2O
B.硫酸铁溶液与氢氧化钡溶液混合:Fe3++S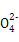 +Ba2++3OH-
+Ba2++3OH- Fe(OH)3↓+BaSO4↓
Fe(OH)3↓+BaSO4↓
C.次氯酸钙溶液中通入过量的CO2:ClO-+H2O+CO2 HC
HC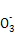 +HClO
+HClO
D.碳酸氢镁与足量的石灰水反应:Mg2++2HC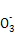 +2OH-+Ca2+
+2OH-+Ca2+ CaCO3↓+MgCO3↓+2H2O
CaCO3↓+MgCO3↓+2H2O
参考答案:C
本题解析:A项,浓硝酸应拆写成离子形式,正确为Cu+4H++2N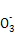
 Cu2++2NO2↑+2H2O;B项,正确的离子方程式应为2Fe3++3S
Cu2++2NO2↑+2H2O;B项,正确的离子方程式应为2Fe3++3S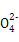 +3Ba2++6OH-
+3Ba2++6OH- 2Fe(OH)3↓+3BaSO4↓;D项,应生成Mg(OH)2沉淀,正确应为:Mg2++2HC
2Fe(OH)3↓+3BaSO4↓;D项,应生成Mg(OH)2沉淀,正确应为:Mg2++2HC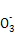 +4OH-+2Ca2+
+4OH-+2Ca2+ Mg(OH)2↓+2CaCO3↓+2H2O。
Mg(OH)2↓+2CaCO3↓+2H2O。
本题难度:一般
3、选择题 下列反应的现象描述与离子方程式都正确的是( )
A.金属镁与稀盐酸反应,有氢气产生:Mg+2H++2Cl-═MgCl2+H2↑
B.氯化钡溶液与稀硫酸反应,有白色沉淀产生:Ba2++SO42-═BaSO4↓
C.碳酸钠溶液与盐酸反应,有气泡逸出:Na2CO3+2H+═2Na++H2O+CO2↑
D.过量铁粉与氯化铁溶液反应,溶液变浅绿色:Fe+Fe3+═2Fe2+
参考答案:A.金属镁与稀盐酸反应,有氢气产生的离子反应为Mg+2H+═Mg2++H2↑,故A错误;
B.氯化钡溶液与稀硫酸反应,有白色沉淀产生的离子反应为Ba2++SO42-═BaSO4↓,故B正确;
C.碳酸钠溶液与盐酸反应,有气泡逸出的离子反应为CO32-+2H+═H2O+CO2↑,故C错误;
D.过量铁粉与氯化铁溶液反应,溶液变浅绿色的离子反应为Fe+2Fe3+═3Fe2+,故D错误;
故选B.
本题解析:
本题难度:一般
4、选择题 化学用语是学习化学的工具和基础.下列有关化学用语的说法或使用正确的是( )
A.稀有气体的晶体,其组成微粒是原子,晶体中不存在分子间作用力
B.核素C-12的原子组成符号为126C,二氧化碳分子的结构式为O=C=O
C.NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O
D.表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=-571.6KJ/mol
参考答案:A、稀有气体是由単原子分子过程的单质气体,分子间存在分子间作用力,故A错误;
B、核素C-12的原子组成符号质子数在左下角,质量数写在左上角,应为126C,二氧化碳分子的结构式为O=C=O,故B错误;
C、NaNO2溶液中加入酸性KMnO4溶液,亚硝酸根离子具有还原性,高锰酸钾具有强氧化性,所以亚硝酸根化合价升高被氧化为硝酸根,高锰酸钾化合价降低被还原为锰离子,结合离子方程式的电荷守恒和原则守恒书写离子方程式为2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O,故C正确;
D、燃烧热是指1mol可燃物质完全燃烧生成稳定氧化物时放出的热量,燃烧热的热化学方程式为H2(g)+12O2(g)=H2O(l)△H=-285.8KJ/mol,故D错误;
故选C.
本题解析:
本题难度:一般
5、选择题 ( 4分) 通常条件下PbSO4是一种不溶于水、酸、碱溶液的白色沉淀。但是PbSO4却溶于CH3COONH4溶液得无色溶液(1)。在(1)溶液中再通入H2S气体形成黑色沉淀(2)。结合中学化学有关离子反应发生的条件、离子反应方程式书写规则,写出(1)(2)两种产物形成的离子方程式:
(1)??;
(2)?。
参考答案:(4分)(1) PbSO4 +2 CH3COO- = Pb(CH3COO)2 + SO42-
(2) Pb(CH3COO)2 + H2S =" PbS↓+" 2CH3COOH
本题解析:(1) PbSO4 +2 CH3COO-=Pb(CH3COO)2+SO42-
(2) Pb(CH3COO)2+H2S=PbS↓+2CH3COOH
PbSO4 、PbS是沉淀,写分子形式,Pb(CH3COO)2难电离,写分子形式,H2S、CH3COOH是弱电解质,写分子形式。
本题难度:简单