1ЎўСЎФсМв Л®ИИ·ЁЦЖұёFe3O4ДЙГЧҝЕБЈөД·ҙУҰКЗ3Fe2Ј«Ј«2S2O ?Ј«O2Ј«xOHЈӯ===Fe3O4Ј«S4O
?Ј«O2Ј«xOHЈӯ===Fe3O4Ј«S4O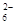 ?Ј«2H2OЈ¬ПВБРЛө·ЁЦРЈ¬ХэИ·өДКЗ(ЎЎЎЎ)
?Ј«2H2OЈ¬ПВБРЛө·ЁЦРЈ¬ХэИ·өДКЗ(ЎЎЎЎ)
AЈ®ГҝЙъіЙ1mol Fe3O4Ј¬·ҙУҰЧӘТЖөДөзЧУЧЬКэОӘ3mol
BЈ®Fe2Ј«әНS2O ¶јКЗ»№ФӯјБ
¶јКЗ»№ФӯјБ
CЈ®1mol Fe2Ј«ұ»Сх»ҜКұЈ¬ұ»Fe2Ј«»№ФӯөДO2өДОпЦКөДБҝОӘ1/3mol
DЈ®xЈҪ2
2ЎўСЎФсМв LiAlH4КЗЦШТӘөДҙўЗвІДБПЈ¬ЖдЧйіЙАаЛЖУЪNa3AlF6ЎЈіЈјыөД№©ЗвФӯАнИзПВГжБҪёц·ҪіМКҪЛщКҫЈә
ўЩ2LiAlH4 2LiHЈ«2AlЈ«3H2Ўь
2LiHЈ«2AlЈ«3H2Ўь
ўЪLiAlH4Ј«2H2O=LiAlO2Ј«4H2Ўь
ПВБРЛө·ЁХэИ·өДКЗ(ЎЎЎЎ)
AЈ®LiAlH4КЗ№ІјЫ»ҜәПОпЈ¬LiHКЗАлЧУ»ҜәПОп
BЈ®ЙъіЙөИЦКБҝөДЗвЖшЈ¬·ҙУҰўЩЎўўЪЧӘТЖөзЧУКэЦ®ұИОӘ4?3
CЈ®Зв»Ҝп®ТІКЗТ»ЦЦҙўЗвІДБПЈ¬№©ЗвФӯАнОӘLiHЈ«H2O=LiOHЈ«H2Ўь
DЈ®Иф·ҙУҰўЩЦРЙъіЙ3.36 LЗвЖшЈ¬ФтТ»¶ЁУР2.7 gВБЙъіЙ
3ЎўСЎФсМв ФЛ¶Ҝ»бЙП·ўБоЗ№ЛщУГЎ°»рТ©ЎұөДЦчТӘіЙ·ЦКЗВИЛбјШәНәмБЧЈ¬ЧІ»чКұ·ўЙъөД»ҜС§·ҙУҰОӘЈә5KC1O3+6P ЈҪ3P2O5+5KC1ЎЈПВБРУР№ШёГ·ҙУҰөДРрКцЦРЈ¬ХэИ·өДКЗ
AЈ®ВИЛбјШКЗ»№ФӯјБ
BЈ®·ҙУҰЦРПыәД3molPКұЈ¬ЧӘТЖөзЧУөДОпЦКөДБҝОӘ15mol
CЈ®KClјИКЗСх»ҜІъОпЈ¬УЦКЗ»№ФӯІъОп
DЈ®·ўБоКұІъЙъөД°ЧСМЦ»КЗKC1№ММеҝЕБЈ
4ЎўСЎФсМв Т»¶ЁМхјюПВЈ¬PbO2УлCr3Ј«·ҙУҰЈ¬ІъОпКЗCr2O72-әНPb2Ј«Ј¬ФтЙъіЙ1 mol Cr2O72-·ҙУҰЛщРиPbO2өДОпЦКөДБҝОӘ
AЈ®3Ј®0 mol
BЈ®1Ј®5 mol
CЈ®1Ј®0 mol
DЈ®0Ј®75 mol
5ЎўСЎФсМв ҫЭПӨЈ¬өЪ16ҪмЦР№ъ№гЦЭСЗФЛ»бФЪЙПК№УГөД·ўБоЗ№ЛщУГөДЎ°»рТ©ЎұіЙ·ЦКЗВИЛбјШәНәмБЧЈ¬ҫӯЧІ»ч·ўіцПмЙщЈ¬Н¬КұІъЙъ°ЧЙ«СМОнЎЈЧІ»чКұ·ўЙъ·ҙУҰөД»ҜС§·ҪіМКҪОӘЈәKClO3+ P-- P2O5+ KCl(ОҙЕдЖҪ)Ј¬ФтПВБРУР№ШРрКцҙнОуөДКЗЈЁ?Ј©
AЈ®ЙПКц·ҙУҰКЗ·ЕИИ·ҙУҰ
BЈ®ІъЙъ°ЧЙ«СМОнөДФӯТтКЗЙъіЙөДP2O5°ЧЙ«№ММеРЎҝЕБЈЈЁСМЈ©ОьЛ®РФәЬЗҝЈ¬ОьКХҝХЖшЦРөДЛ®·ЦЈ¬ЙъіЙБЧЛбРЎТәөОЈЁОнЈ©
CЈ®ёГ·ҙУҰСх»ҜјБУл»№ФӯјБОпЦКөДБҝЦ®ұИОӘ6Јә5
DЈ®ЙПКц·ҙУҰЦРПыәД3molPКұЈ¬ЧӘТЖөзЧУөДОпЦКөДБҝОӘ15mol