1、选择题 实际存在的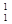 H、
H、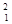 H、
H、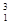 H、H―和H,它们是
H、H―和H,它们是
A.氢的五种同位素
B.五种氢元素
C.氢的五种原子
D.氢元素的五种不同微粒
参考答案:D
本题解析:A错,同位素是指质子相同则中子数不同的同一元素不同原子;B错,氢元素只有一种;C错,H―为氢离子;D正确;
本题难度:简单
2、选择题 Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X焰色黄色。五种元素核电荷数之和为54,最外层电子数之和为20。W、Z最外层电子数相同Z的核电荷数是W的2倍。工业上一般通过电解氧化物法获得Y单质。则下列说法不正确的(? )
A.X和Y的最高价氧化物对应的水化物之间可发生反应
B.Q和W可形成原子个数比为1:1和1:2的常见化合物
C.Y和Z所形成的化合物与水反应既有气体有有沉淀生成
D.X和W之间可形成阴阳离子个数比为1:1和1:2的常见化合物
参考答案:D
本题解析:X焰色黄色则X是Na;Q、W、X、Y、Z是原子序数依次增大的短周期元素,W、Z最外层电子数相同Z的核电荷数是W的2倍。则W是O;Z是S;X、Y是金属元素,工业上一般通过电解氧化物法获得Y单质。则Y是Al;五种元素核电荷数之和为54,最外层电子数之和为20。则Q是C.即这五种元素分别是:C? O? Na? Al? S。A.NaOH是强碱,Al(OH)3是两性氢氧化物,二者可发生反应生成偏铝酸钠和水。正确。BQ和W可形成CO 和CO2。正确。C.Al2S3是弱酸弱碱盐,在水中发生双水解反应产生氢氧化铝沉淀和硫化氢气体。正确。D.X和W之间可形成Na2O 、Na2O2两种常见化合物,它们的阴阳离子个数比都是为2:1.错误。
本题难度:一般
3、选择题 下列性质的比较中,正确的是
A.碱性:KOH>NaOH>Mg(OH)2>Ca(OH)2
B.沸点:HF<HCl<HBr<HI
C.热稳定性:CH4>PH3>H2O>HF
D.酸性:HClO4>H2SO4>H3PO4>H2SiO3
参考答案:D
本题解析:金属性越强,最高价氧化物的水化物的碱性越强,金属性是K>Ca>Na>Mg,A不正确。氟化氢中含有氢键沸点高于碘化氢的,B不正确。非金属性越强,相应氢化物的稳定性越强,非金属性是F>O>C>Si,C不正确。非金属性越强,,最高价氧化物的水化物的酸性越强,因此正确的答案是D。
本题难度:一般
4、选择题 下列物质中氧元素的化合价正确的是
A.H2O2中氧元素的化合价为-2
B.O2中氧元素的化合价为-2
C.NaOH中氧元素的化合价为-1
D.Na2O中氧元素的化合价为-2
参考答案:D
本题解析:过氧化氢中H是+1价的,所以O是-1价的,A错误。单质是0价的,B不正确。氢氧化钠中Na和H都是+1价的,所以O是-2价的,C不正确。氧化钠中Ns是+1价的,因此O是-2价的,正确。答案是D。
本题难度:简单
5、选择题 下列关于电子云的说法中不正确的是(?)
A.s电子绕核旋转,其轨道为一圆圈,而p电子是走“8”字形
B.s轨道是球形轨道
C.轨道不同,电子云的形状也不一样
D.电子云图是形象地描述电子在空间单位体积内出现概率大小的图形
参考答案:A
本题解析:A、电子的运动轨道是不确定的,圆圈、“8”字形都是电子云的形状
点评:此题考核了电子云的相关概念,属于基础题。
本题难度:简单