1��ѡ���� �������з�Ӧ���Խ�����ת��Ϊ���ȴ�99.9%�ĸߴ�����
��Ӧһ��Ni���֣�s��+4CO��g��
Ni��CO��4��g����H��0
��Ӧ����Ni��CO��4��g��Ni������s��+4CO��g����H��0
����˵��������ǣ�������
A�����ڷ�Ӧһ���ʵ�����ѹǿ��������Ni��CO��4������
B���ᴿ�����У�CO�����ѭ��ʹ��
C�������¶ȣ���Ӧһ�ķ�Ӧ���ʼ�С����Ӧ������������
D���Է�Ӧ������180-200�棬�¶�Խ�ߣ�Ni��CO��4��g����ת����Խ��
2������� �����ж�����Ӧ����Fe��s��+CO2��g���TFeO��s��+CO��g����ƽ�ⳣ��ΪK1��
��Fe��s��+H2O��g���TFeO��s��+H2��g����ƽ�ⳣ��ΪK2������ڲ�ͬ�¶��£�K1��K2ֵ���£�
| �¶�/�� | K1 | K2
500
1.00
3.15
700
1.50
2.25
900
2.50
1.50
|
��1����500��ʱ���з�Ӧ�٣�CO2��ʼŨ��Ϊ2mol/L��CO2��ת����Ϊ______��
��2����һ�����Ϊ10L���ܱ������У�����������Fe��FeO��ĩ��Ȼ��
���ٳ���CO2��H2O��g����1mol������һ�����¶ȣ����϶�����Ӧͬʱ�ﵽƽ�⣮��______����ֵ���
���ٳ���CO22mol��H2?4mol��������900�棬���϶�����Ӧ�ﵽƽ�����ƽ��ʱ�������������______��
3��ѡ���� ���ڿ��淴Ӧ��3A(g)+B(g) C(s)+4D(g)?(����ӦΪ���ȷ�Ӧ��������������ȷ���ǣ�A%ָƽ��ʱ���������A�İٷֺ�����
C(s)+4D(g)?(����ӦΪ���ȷ�Ӧ��������������ȷ���ǣ�A%ָƽ��ʱ���������A�İٷֺ�����
[? ]
A.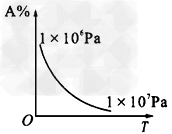
B.
C.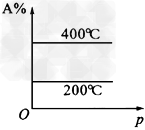
D.
4��ѡ���� ��ͼI��ʾ���ס���֮��ĸ���K�ͻ���F�����������ƶ������г���2 molA��l mol B�����г���2mol C��1 mol He����ʱKͣ��0������һ�������·�����Ӧ��2A(g)+ B(g)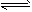 2C(g)����Ӧ�ﵽƽ����ٻָ���ԭ�¶ȣ�������˵����ȷ����
2C(g)����Ӧ�ﵽƽ����ٻָ���ԭ�¶ȣ�������˵����ȷ����

[? ]
A. �ﵽƽ��ʱ������K����ͣ���ڿ̶�0��-2֮��
B. ���ﵽƽ��ʱ������K����ͣ���ڿ̶�-1����������C��ת����С��50%
C. ���ﵽƽ��ʱ������K����ͣ���ڿ����̶�-2����������F����ͣ���̶ȴ���4
D. ��ͼI��x���ʾʱ�䣬��y��ɱ�ʾ�ס���������������������ʵ�����A �����ʵ���
5��ѡ���� ����ʹ2NO2��g��?N2O4��g��ƽ����ϵ��NO2��N2O4Ũ�ȵı�ֵ��С�Ĵ�ʩ�ǣ�������
A���¶ȡ�������䣬ͨ��NO2
B���¶ȡ�������䣬ͨ��N2O4
C���¶ȡ�������䣬���뵪��
D���¶Ȳ��䣬��С�������