1��ѡ���� ��Ӧ2A��g��?2B��g��+E��g����H��0���ﵽƽ��ʱ��Ҫʹ����Ӧ���ʽ��ͣ�A��Ũ������Ӧ��ȡ�Ĵ�ʩ�ǣ�������
A����ѹ
B����ѹ
C����СE��Ũ��
D������
2��ѡ���� �ڹ̶��ݻ���������ʢ��1molPCl5��200��ʱ�������·�Ӧ��PCl5��g��?PCl3+Cl2��g���ﵽƽ��ʱ��PCl5�������ΪM%������ͬһ�¶Ⱥ�ͬһ�����У����Ͷ��2molPCl5����ƽ��ʱ��PCl5��ռ�������ΪN%����M��N�Ĺ�ϵ�ǣ�������
A��M��N
B��M��N
C��M=N
D�����Ƚ�
3������� ��ӦA(g)+B(g)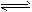 C(g) +D(g)�����е������仯��ͼ��ʾ���ش��������⡣
C(g) +D(g)�����е������仯��ͼ��ʾ���ش��������⡣
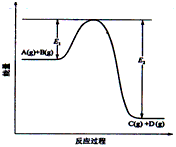
��1���÷�Ӧ��_____________��Ӧ(����ȡ������ȡ�)
��2������Ӧ�ﵽƽ��ʱ�������¶ȣ�A��ת����______(�������С�������䡱)��ԭ����________________________________________��
��3����Ӧ��ϵ�м�������Է�Ӧ���Ƿ���Ӱ��?________��ԭ����_________________________
��4���ڷ�Ӧ��ϵ�м����������Ӧ��������E1��E2�ı仯�ǣ�E1_________��E2________(�������С���������䡱)��
4��ѡ���� �ں���ʱ��һ�̶��ݻ��������ڷ������·�Ӧ��2NO2��g��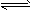 N2O4(g)�ﵽƽ��ʱ������������ͨ��һ������NO2��g�������´ﵽƽ������һ��ƽ��ʱ��ȣ�NO2���������
N2O4(g)�ﵽƽ��ʱ������������ͨ��һ������NO2��g�������´ﵽƽ������һ��ƽ��ʱ��ȣ�NO2���������
[? ]
A������
B������
C����С
D�����ж�
5������� ��80��ʱ����0.40mol��N2O4�������1L�̶��ݻ����ܱ������з�����Ӧ��N2O4�T2NO2����H��0����ÿ��һ��ʱ��������ڵ����ʽ��вⶨ���õ��������ݣ�
| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 | 100
n��N2O4����mol��
0.40
a
0.20
c
d
e
n��NO2����mol��
0.00
0.24
b
0.52
0.60
0.60
|
��1����20s-40s֮�䣬��N2O4��ʾ��ƽ����Ӧ����Ϊ______��
��2����80��ʱ�÷�Ӧ��ƽ�ⳣ��K=______��
��3��Ҫ����÷�Ӧ��ƽ�ⳣ�����ɲ�ȡ�Ĵ�ʩ�У�����ţ�______��
������N2O4����ʼŨ��?������������ͨ��NO2
��ʹ�ø�Ч����?�������¶�
��4����Ӧ������100s���������¶ȣ�����������ɫ______�����dz������������䡱����
��5����Ӧ������100s�������������ٳ���0.40mol��N2O4���壬��ﵽ��ƽ���N2O4��ת���ʽ�______�����������С�����䡱����