1��ѡ���� �йغϽ��˵���������? (? )
A��Ӳ������
B���۵㽵��
C����������ǿ
D���������
�ο��𰸣�C
����������Ͻ���۵��������ֵ��۵㣬����е���ܻ���ǿ�����н����������������ԣ��ʴ�ΪC
�����Ѷȣ���
2��ѡ���� ����˵���������
A������KSCN���Լ���Fe2+
B��������NaOH��Һ����Fe3+
C��ͨ�����Ϸ�Ӧ���Եõ�Fe(OH)3
D��ͨ�����Ϸ�Ӧ���Եõ�FeCl2
�ο��𰸣�A
���������A��KSCN��Һ���Ȼ��������û��ʵ������Ҫ�����������ӣ�����Ҫ���������������ȣ�A����ȷ��B������������Һ�������ӷ�Ӧ���ɺ��ɫ�����������������Լ��������ӣ�B��ȷ��C��������������������ˮ�������Ϸ�Ӧ��������������C��ȷ��D���Ȼ��������������Ϸ�Ӧ�����Ȼ�������D��ȷ����ѡA��
�����Ѷȣ���
3��ѡ���� ����������ȷ����
A���������Ż�ʱ���ô���ˮ�������
B�����Ʋ;߿ɴ������Ʋ;߳�ʱ�������ԡ�����ʳ��
C����50mL��Ͳ������0.1mol��L-1̼������Һ
D����ȼ���ױ�ҩƷ����ǿ�����Ե�����Ҫ�ֿ����ò�Զ���Դ
�ο��𰸣�D
���������ѡ��A������������ˮ��Ӧ�ų��������������п�ȼ�ԣ���˽������Ż�����ˮ��𡣿���ɳ������
ѡ��B���������Խ�����������Ӧ����˲��ɴ�����ԡ�����ʳ�
ѡ��C��������ҺӦ���ձ�������ƿ�����ƣ���Ͳֻ��������ȡҺ�����������ϣ���ΪD��
���������⿼����ʵ���Ұ�ȫ���⣬�ȿ�����ѧ���Ļ���֪ʶ����������ѧ����ʵ�鰲ȫ��ʶ�������е��⡣
�����Ѷȣ���
4��ʵ���� �����仯���������������������Ź㷺��Ӧ�á�ijʵ��С�����������ʵ��̽��
ijЩ������������Ʊ�����ɡ����ʵȡ��밴Ҫ��ش��������⣺
��1�������Ȼ�����Ʊ�����ɣ���ʵ�����У�FeCl2����________�����ᷴӦ�Ʊ���FeCl3�������ۺ�
________��Ӧ�Ʊ�������һ����FeCl2��FeCl3�Ļ������Ʒ�����n(Fe)��n��Cl��=1��2.2�������
Ʒ��FeCl2��FeC13���ʵ���֮��Ϊ__________��
��2��ˮ��������������ز��ϨD�D������أ�K2FeO4�����Ʊ���Ӧ�ã�
FeC13��KClO��ǿ���������·�Ӧ����ȡK2FeO4���䷴Ӧ�����ӷ���ʽΪ
________________________________________________________________________��
��MnO2��Zn������ƣ�K2FeO4��ZnҲ������ɼ��Ե�أ��������缫��ӦʽΪ
________________________________________________________________________��
��3���������������������ؾ��壨K3[Fe(C2O4)3�ݡ�xH2O������Ԫ�غ����IJⶨ��
����һ������10.00 g�����������ؾ��壬���Ƴ�250 mL��Һ��
�������ȡ������Һ25.00 mL����ƿ�У���ϡH2SO4�ữ���μ�KMnO4��Һ�������ǡ��ȫ�������ɶ�����̼��ͬʱMnO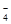 ����ԭ��Mn2+����Ӧ�����Һ�м�������п�ۣ�����ɫ�պ���ʧ��������Һ�ռ�����ƿ�У���ʱ��Һ�Գ����ԡ�
����ԭ��Mn2+����Ӧ�����Һ�м�������п�ۣ�����ɫ�պ���ʧ��������Һ�ռ�����ƿ�У���ʱ��Һ�Գ����ԡ�
����������0.0200 mol/L KMnO4��Һ�ζ������������Һ���յ㣬����KMnO4��Һ20.02 mL���ζ���MnO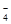 ��ԭ��Mn2+��
��ԭ��Mn2+��
�ظ��������������������������0.0200 mol/L KMnO4��Һ19.98 mL��
�ٲ���һ�г���Ͳ�����������ձ��⣬����Ҫ�IJ���������____________________���������ζ�������ʢװKMn4��Һ����������Ϊ___________���������һ����Һʱ����ƿ����Һ��Ϊ_________ɫ�����ð������Һ��ɫ���ٱ仯��ȷ��Ϊ�ζ��յ㡣
�ڲ��������п�۵�Ŀ����_______________________________��
д��п���뷴Ӧ�����ӷ���ʽ��____________________________________________��
��ʵ���øþ�������Ԫ�ص���������Ϊ____________���ڲ�����У��������KMnO4��Һ�������㣬���õ���Ԫ�غ���____________�����ƫ�͡���ƫ�ߡ�����Ӱ�족��
�ο��𰸣���18�֣���1������?���� ��2�֣���4��1��2�֣�
��2��2Fe3����3ClO����10OH����2FeO42����3Cl����5H2O��2�֣�
FeO42����3e����4H2O��Fe(OH)3����5OH����2�֣�
��3����250ml����ƿ�ͽ�ͷ�ιܣ�2�֣�����ʽ�ζ���?�죨2�֣�
�ڽ�Fe3����ԭ��Fe2����1�֣���Zn��2Fe3����Zn2����2Fe2����2�֣�?��11.2%��2�֣�?ƫ�ߣ�1�֣�
�����������1�����DZ�۽�������ǿ��������Ӧ���ɣ�3������������������Ӧ���ɣ�2������������ʵ�����У�FeCl2�����������ᷴӦ�Ʊ���FeCl3�������ۺ�������Ӧ�Ʊ�������Ʒ��FeCl2��FeC13���ʵ����ֱ���x ��y������ݻ����n(Fe)��n��Cl����1��2.2��֪����x��y��:��2x��3y����1��2.2�����x��y��4��1��
��2��FeC13��KClO��ǿ���������·�Ӧ����ȡK2FeO4���ڷ�Ӧ����Ԫ�صĻ��ϼ۴ӣ�1�۽��͵���1�ۣ��õ�2�����ӡ���Ԫ�صĻ��ϼ۴ӣ�3�����ߵ���6�ۣ�ʧȥ3�����ӣ�����ԭ���������������ʵ���֮����2:3����˸÷�Ӧ�����ӷ���ʽΪ2Fe3����3ClO����10OH����2FeO42����3Cl����5H2O��ԭ����������õ����ӣ�������K2FeO4��Zn���Ե���У�п�Ǹ�����K2FeO4�����������������缫��ӦʽΪFeO42����3e����4H2O��Fe(OH)3����5OH����
��3��������һ�����ʵ���Ũ����Һʱ������Ͳ�����������ձ��⣬����Ҫ�IJ���������250ml����ƿ�Ͷ��ݵĽ�ͷ�ιܡ����ڸ��������Һ����ǿ�����ԣ��������ԣ����Բ������ζ�������ʢװKMn4��Һ����������Ϊ��ʽ�ζ��ܣ����Ը��������Һ�Ժ�ɫ�����Ե������һ����Һʱ����ƿ����Һ��Ϊ��ɫ�����ð������Һ��ɫ���ٱ仯��ȷ��Ϊ�ζ��յ㡣
���������Ը��������ҺҲ�ܰ����������������������ӣ����Լ���п�۵������ǽ�Fe3����ԭ��Fe2������Ӧ�����ӷ���ʽΪZn��2Fe3����Zn2����2Fe2����
������ʵ��������0.0200 mol/L KMnO4��Һ��ƽ��ֵ����20.02 mL�� 19.98 mL����2��20.00ml���������ĸ�����ص����ʵ�����0.0200L��0.0200 mol/L��0.0004mol�����ݵ��ӵ�ʧ�غ��֪����Һ���������ӵ����ʵ�����0.0004mol��5��0.0020mol�����Ըþ�������Ԫ�ص���������Ϊ ��100%��11.2%���ڲ�����У��������KMnO4��Һ�������㣬����ܵ��²����ʣ�࣬�Ӷ����µ����������ĸ��������Һ��������ӣ��Ӷ�������Ԫ�صĺ���ƫ�ߡ�
��100%��11.2%���ڲ�����У��������KMnO4��Һ�������㣬����ܵ��²����ʣ�࣬�Ӷ����µ����������ĸ��������Һ��������ӣ��Ӷ�������Ԫ�صĺ���ƫ�ߡ�
�����Ѷȣ�����
5��ѡ���� �ں���Cu��NO3��2��Mg��NO3��2��AgNO3����Һ�м�������п�ۣ������û������ǣ�?��
A��Mg
B��Cu
C��Ag
D��H2
�ο��𰸣�C
�����������
�����Ѷȣ�һ��