1��ѡ���� ��������������غ�����[KAl(SO4)2��12H2O]�Ļ��Һ�У����SO42-��Ũ��Ϊ0.4mol/L������������0.4mol/L KOH��Һʱ�����ɳ���ǡ����ȫ�ܽ⣬��Ӧ������Һ��K+Ũ��ԼΪ
[? ]
A��0.225mol/L
B��0.25mol/L
C��0.45mol/L
D��0.5mol/L
2������� �ӻ��յĺ�ͭ���·�������ȡͭʱ����������������ַ������ش��й����⡣
�����ף�?
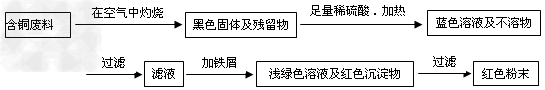
�����ң�?
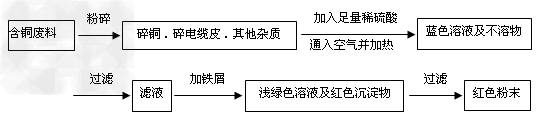
��1�����������У����ϵ�ǰ��������ɫ��ѧ������Ƿ���______��������?_________��
��2����������ͭ�ܽ�������ɫ��Һʱ������Ӧ�����ӷ���ʽΪ_____________________________������������ɫ��ѧҪ���ܽ�ͭ��������ͭʱ�����ɽ���������ֶ�μ��뵽ͭ����ϡ����Ļ�����У�����ʹͭ�ܽ���ȫ�����������������������ʵ���֮�����Ϊ��_________�U__________��
��3��Ϊ�����ԭ�ϵ�������,���һ������dz��ɫ��Һͨ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ���Ȼ����ɵõ�һ�ֽᾧˮ����ľ��塣��þ���������м�⣺
����ȡa?g�ľ��������ˮʵ�飬�����ˮ����Ϊ��a��1��26��g ?
�ڽ���ˮ��������������ˮ�����Һ��μ�1��00mol/L���Ȼ�����Һ�����μ�10��00mL��Һʱ������ǡ����ȫ��ͨ�������֪�þ���Ļ�ѧʽ��?___________��
��4���Ȼ���ͭ��CuCl������Ҫ�Ļ���ԭ�ϡ����ұ��涨�ϸ��CuCl��Ʒ����Ҫ����ָ��ΪCuCl��������������96.5%?����ҵ��������ͭ��ԭ�ϳ�ͨ�����з�Ӧ�Ʊ�CuCl?��
2CuSO4+?Na2SO3?+?2?NaCl?+?Na2CO3?=?2?CuCl?��+?3?Na2SO4?+?CO2�� �ⶨCuCl��������ʱ��ȷ��ȡ���Ʊ���0.2500g?CuCl��Ʒ����һ������0.5mol��L-1?FeCl3?��Һ�У�����Ʒ��ȫ�ܽ��ˮ20mL����0.1000mol��L-1?Ce��SO4��2��Һ�ζ����յ㣬����24.60mL?Ce��SO4��2��Һ���йط�Ӧ�����ӷ���ʽΪ��?
Fe3+ +CuCl=Fe2+ +Cu2+ +Cl-?��Ce4+?+?Fe?2+?=?Fe?3+?+?Ce3+ ?ͨ������˵��������Ʒ��CuCl�����������Ƿ���ϱ���
3������� ��������Ҫ�ɷ���FeS2 ��ij���᳧�ڽ��л�����ɷֲⶨʱ��ȡ0.1000 g��Ʒ�ڿ����г�����գ������ɵ�SO2����������Fe2(SO4)3��Һ��ȫ��Ӧ����Ũ��Ϊ0.02000 mol��L��K2Cr2O7����Һ�ζ����յ㣬����K2Cr2O7��Һ25.00 mL ����֪��SO2 + 2Fe3+ + 2H2O == SO42- + 2Fe2+ + 4H+
Cr2O72-+ 6 Fe2+ + 14 H+ == 2 Cr3+ + 6 Fe3+ + 7 H2O
��1����Ʒ��FeS2�����������ǣ��������ʲ��μӷ�Ӧ��________________��
��2��������6 g FeS2������SO2ȫ��ת��ΪSO3����ʱ�ų�9.83 kJ������������SO3��ˮȫ����������H2SO4 ���ų�13.03 kJ������д��SO3����ת��ΪH2SO4���Ȼ�ѧ����ʽ��______________________________________________________________________��
?��3������10 t���������������ϲ���SO2���������״����Ϊ_______________L���Ƶ�98������������Ϊ__________ t ��SO2ȫ��ת��ΪH2SO4ʱ�ų���������_______ kJ��
4�������� ij50 mL��Һ��0.20 mol/L Al2(SO4)3��0.005 mol/L H2SO4�������Һ�еμ�0.40 mol/L��NaOH ��Һֱ�����ɵij��������ܽ���ʧ���Լ��㣺
(1)��ʼ����ʱ������NaOH��Һ�������
(2)���ɳ����������ʱ�����NaOH��Һ�������
(3)������ȫ�ܽ�ʱ������NaOH��Һ����С�����
5������� ������NOx��NO��NO2�Ļ�������N2O4����
��1�����ݷ����ŷű���1m3�������������400 mg NOx����NOx��NO��������Ϊ0. 85����1m3���������������NO_________L����״��������2λС ������
��2����ҵ��ͨ����������������Ϊ0.150��Na2CO3ˮ��Һ���ܶ�1.16 g/mL����ΪNOx���ռ�����̼������Һ���ʵ���Ũ��Ϊ___________mol/L(����2λС��)��
��3����֪��
NO+NO2+Na2CO3��2NaNO2+CO2 ��
2NO2+Na2CO3��NaNO2+ NaNO3+CO2 ��
1m3��2000 mg NOx����������������Ϊ0.150��̼������Һ���ա���������Ϊ80%�����պ������______�ŷű�������ϡ������ϡ��������ɣ�______________________
��4����������ɸı�������NO��NO2�ıȣ���ӦΪ��NO+2HNO3��3NO2+H2O��������n(NO):n(NO2)=2��3ʱ����������ߡ�1m3������2000 mg NOx������n(NO):n(NO2) =9:1��
���㣺
(I)Ϊ�˴ﵽ��������ʣ�1m3����������������ʵ���������3λС������
(��)1m3�����ﵽ���������90%ʱ�����պ�����NaNO3�������������������շ�Ӧ�У���Ӧ�ٱȷ�Ӧ��Ѹ�١�����������lλС������