1、选择题 氯元素 的相对原子质量为35.5,由23Na、35Cl、37Cl构成的11.7g氯化钠中,37Cl的质量为
的相对原子质量为35.5,由23Na、35Cl、37Cl构成的11.7g氯化钠中,37Cl的质量为
A.1.75g? B.1.85 g? C.5.25 g? D .5.85g
.5.85g
参考答案:B
本题解析:略
本题难度:一般
2、选择题 下列表示方法正确的是
A.铜的原子结构示意图: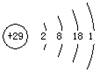
B.S2- 核外电子排布式:[Ne] 2s23p6
C.O原子处于基态的轨道表示式: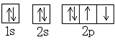
D.用电子式表示MgCl2的形成:Mg:+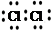 →
→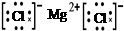
参考答案:A
本题解析:硫离子的最外层电子数是8个,B不正确;C不正确,不符合洪特规则;D不正确,应该是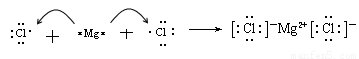 ,答案选A。
,答案选A。
本题难度:简单
3、选择题 以下各种表示式中,最能反映氮原子核外电子运动状态的是?(?)
A.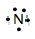
B.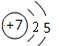
C.1s22s22p3
D.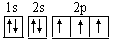
参考答案:D
本题解析:
A、只表示最外层;B、只表示分两个电子层;C、不能表示电子自旋方向;D、全面表示出电子的电子层、所在的能级、轨道、电子的自旋方向,D正确。
本题难度:简单
4、选择题 在下列各项叙述中,你认为正确的是( )
A.构成单质分子的微粒一定含有共价键
B.在NaCl中,除存在Na+和Cl-的静 电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用
C.HF的稳定性较强,是因为其分子间能形成氢键
D.含有共价键的物质一定是共价化合物
参考答案:B
本题解析:稀有气体单质不含化学键,A不正确。氟元素是最活泼的非金属元素,形成的氢化物稳定,而与氢键无关,氢键一般影响稳定的沸点,C不正确。含有共价键的物质可能是单质也可能是离子化合物,D不正确。答案选B。
本题难度:一般
5、选择题 下列各组微粒中,电子总数相同的是( )
A.F-、Cl-、Br-、I-
B.S2-、Ca2+、Ar、Cl-
C.Na+、K+、Mg2+、Al3+
D.Mg2+、Mg、Al3+、Al
参考答案:B
本题解析:A项电子总数分别10、18、36、54;B项均为18;C项10、18、10、10;D项10、12、10、13.B正确。
本题难度:简单