1、选择题 由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH =1,c(Al3+)=0.4 mol・L-1,c(SO42-)=0.8 mol・L-1,, 则c(K+)为
[? ]
A. 0.15 mol・L-1
B. 0.2 mol・L-1
C. 0.3 mol・L-1
D. 0.4 mol・L-1
参考答案:C
本题解析:
本题难度:简单
2、计算题 (8分)常温下,将20.0 g 14%的NaCl溶液跟30.0 g 24%的NaCl溶液混合,得到密度为1.17 g/cm3的混合溶液。计算:
(1)该混合溶液中NaCl的质量分数。(3分)
(2)该混合溶液中NaCl的物质的量浓度。(3分)
(3)在1000 g水中需加入________摩尔氯化钠,才能使其浓度恰好与上述混合溶液浓度相等。(保留1位小数)(2分)
参考答案:(1)20%、 (2)4mol/L、 (3)4. 3
本题解析:①将20.0g14%的NaCl溶液跟30.0g24%的NaCl溶液混合,混合后溶液的质量为20g+30g=50g,
设混合后NaCl的质量分数为ω,则:50g×ω=20g×14%+30g×24%,解得ω=20%
答:混合后NaCl溶液的质量分数为20%。
②混合后溶液中NaCl的物质的量浓度为 mol/L=4mol/L,
mol/L=4mol/L,
答:混合后氯化钠溶液的物质的量浓度为4mol/L.
③令需要氯化钠的物质的量为n mol,NaCl的质量为n mol×58.5g/mol="58.5n" g,则:
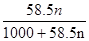 =20%,解得n=4.3,
=20%,解得n=4.3,
答:在1000g水中需要加入4.3 mol NaCl。
考点:考查物质的量的相关计算。
本题难度:一般
3、选择题 设阿伏加德罗常数的值为NA,下列说法中正确的是:
A.1mol苯乙烯中含有的C=C数为4NA
B.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
C.0.1molCnH2n+2中含有的C-C键数为0.1nNA
D.标准状况下,2.24LCHCl3含有的分子数为0.1NA
参考答案:B
本题解析:略
本题难度:简单
4、选择题 把100?g某NaOH溶液(密度为1.22?g/cm3),蒸发浓缩至50?mL时物质的量浓度为8?mol/L,则原溶液的物质的量浓度为
[? ]
A.160?g/L?
B.3.28?mol/L?
C.4.88?mol/L?
D.16%
参考答案:C
本题解析:
本题难度:简单
5、选择题 设NA表示阿伏加得德罗常数的数值,下列叙述中正确的是(?)
A.标准状况下,22.4LH2O中所含有的氢 原子数为2NA
原子数为2NA
B.常温常压下,22 .4L氧气所含的原子数为2NA
C.常温常压下,32 g O2所含的氧原子数为2NA
D.0.1 mol/LNaCl溶液中所含的Na+数为NA
参考答案:C
本题解析:略
本题难度:一般