1、选择题 下列关于热化学反应的描述中正确的是
[? ]
A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283. 0kJ/mol,则表示CO燃烧热的热化学方程为CO(g) +1/2O2(g)=CO2(g) △H=-283.0 kJ.mol-1
C.需要加热才能发生的反应一定是吸热反应
D.1 mol硫燃烧生成气态三氧化硫所放出的热量是硫磺的燃烧热
参考答案:B
本题解析:
本题难度:一般
2、选择题 常温时,下列各溶液中有关粒子浓度的说法正确的是(? )
A.pH=5的NaHSO3溶液:c(HSO3-) > c(SO32-)> c(H2SO3)
B.pH=3的盐酸跟pH=11的氨水等体积混合: c(H+)>c(OH-)
C.pH<7的CH3COONa和CH3COOH的混合溶液 c(Na+)> c(CH3COO-)> c(H+)>c(OH-)
D.pH=12的NaOH溶液中:c(OH-)水电离=1.0×10-12 mol/L
参考答案:AD
本题解析: A项的NaHSO3溶液pH=5,溶液显酸性,说明HSO3- 的电离大于水解,所以c(HSO3-) > c(SO32-)> c(H2SO3),A正确;B项pH=3的盐酸与pH=11的氨水有c(H+)=c(OH-),所以等体积混合氨水过量,所以混合后溶液显碱性c(H+)<c(OH-),B错误;CH3COONa和CH3COOH的混合溶液中有离子电荷守恒式c(Na+)+ c(H+) = c(CH3COO-)+c(OH-),由于pH<7,所以c(H+)<c(OH-),因此有c(Na+)< c(CH3COO-),故C错误;pH=12的NaOH溶液中水的电离受到抑制,但利用水的离子积可计算得溶液中的c(H+)=1.0×10-12 mol/L,所以c(OH-)水电离= c(H+)=1.0×10-12 mol/L,所以D正确。故选AD。
本题难度:一般
3、选择题 常温时,将V1mLcl mol/L的氨水滴加到V2mL c2 mol/L的盐酸中,下列结论正确的是
A.若Vl=V2,cl=c2,则溶液中一定存在c(H+)=c(OH-),是中性
B.若混合溶液的pH=7,则溶液中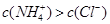
C.若混合溶液的pH=7,则一定存在c1V1>c2V2关系
D.若V1=V2,并且混合液的pH<7,则一定是由于盐酸过量而造成的
参考答案:C
本题解析:A:若Vl=V2,cl=c2,则酸碱恰好中和,生成NH4Cl溶液,由于NH4+的水解,溶液呈酸性,不正确
B:溶液中一定存在电荷守恒c(H+)+c(NH4+)=c(OH-)c(Cl-),当pH=7时,c(H+)=c(OH-),必然有c(NH4+)=c(Cl-),不正确
C:当盐酸过量或恰好中和时,混合溶液均呈酸性,当混合溶液的pH=7,氨水一定过量,即一定存在c1V1>c2V2,正确
D:当Vl=V2,cl=c2时,酸碱恰好中和,溶液水解呈酸性,pH<7,排除
本题难度:一般
4、选择题 根据下列各图曲线表征的信息,得出的结论不正确的是
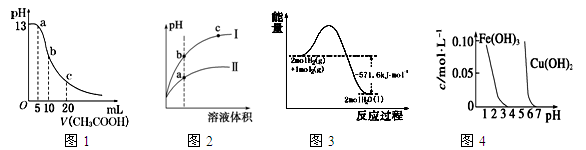
A.图1表示常温下向体积为10 mL 0.1 mol・L-1 NaOH溶液中逐滴加入0.1 mol・L-1 CH3COOH溶液后溶液的pH变化曲线,则b点处有:c(CH3COOH)+c(H+)=c(OH-)
B.图2表示用水稀释pH相同的盐酸和醋酸时溶液的pH变化曲线,其中Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a
C.图3表示H2与O2发生反应过程中的能量变化,H2的燃烧热为285.8 kJ・mol-1
D.由图4得出若除去CuSO4溶液中的Fe3+,可采用向溶液中加入适量CuO,调节溶液的pH至4左右