1、选择题 下列叙述中正确的是( )
A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同
B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C.两原子,如果核外电子排布相同,则一定属于同种元素
D.阴离子的核外电子排布一定与上一周期稀有气体元素原子的核外电子排布相同
参考答案:C
本题解析:
本题难度:简单
2、选择题 有X、Y、Z三种元素,X和Y可以形成XY和XY2两种化合物;Z与X、Y分别形成XZ4和Z2Y两种化合物,在这两种化合物中总电子数均为10个.则X、Y、Z三种元素分别是( )
A.C、N、O
B.C、O、H
C.C、H、O
D.H、N、O
参考答案:B
本题解析:
本题难度:简单
3、简答题 (1)多电子原子核外电子能量是不同的,其中能层序数(n)越小,该能层能量______,在同一能层中,各能级的能量按ns、np、nd、nf的次序______.
(2)原子的电子排布遵循构造原理能使整个原子的能量处于最低状态,处于最低能量的原子叫做______原子,当这些原子______能量后电子跃迁到较高能级后就变成激发态.
(3)如图是周期表中短周期主族元素的一部分,其中电负性最大的元素是______.第一电离能最小的元素是______.
参考答案:(1)能层序数(n)越小,电子离核越近,能量越低,在同一能层中,各能级的能量按ns、np、nd、nf的次序递增,故答案为:越低;递增;
(2)处于最低能量的原子叫做基态原子,激发态能量较高,基态电子跃迁到激发态,需要吸收能量,故答案为:基态;吸收;
(3)同周期:从左到右,元素的电负性逐渐增大.同主族:从上到下,元素的电负性逐渐减小则B的电负性最大,第一电离能的变化与元素原子的核外电子排布有关,通常情况下,当原子核外的电子排布的能量相等的轨道上形成全空,半满,全满的结构时,原子的能量较低,原子较稳定,则该原子比较难失去电子,故第一电离能较大,N的第一电离能大于O,由于元素的种类没有确定,则第一电离能最小的元素可能为C或D,
故答案为:B;C或D.
本题解析:
本题难度:一般
4、填空题 下表列出了核电荷数为21~25的元素的最高正化合价,回答下列问题
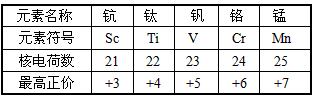
(1)写出下列元素基态原子的核外电子排布式:
Sc________ Ti________ V________ Mn________
(2)已知基态铬原子的电子排布是1s22s22p63s23p63d54s1,并不符合构造原理。人们常常会碰到客观事实与理论不相吻合的问题,当你遇到这样的问题时,你的态度是:______________________
(3)对比上述五种元素原子的核外电子排布与元素的最高正化合价,你发现的规律是________________;出现这一现象的原因是_______________________。
参考答案:(1)Sc: 1s22s22p63s23p63d14s2或[Ar]3d14s2;Ti: 1s22s22p63s23p63d24s2或[Ar]3d24s2;
V: 1s22s22p63s23p63d34s2或[Ar]3d34s2;Mn: 1s22s22p63s23p63d54s2或[Ar]3d54s2
(2)尊重客观事实,注重理论适用范围
(3)五种元素的最高正化合价数值等于各元素基态原子的最高能层s电子和次高能层d电子数目之和;能级交错使得d层电子也参与了化学反应
本题解析:
本题难度:一般
5、选择题 在第n电子层中,当它作为原子的最外层时,容纳电子数最多与第(n-1)层相同;当它作为原子的次外层时,其电子数比(n-1)层多10个,则对此电子层的判断正确的是
[? ]
A.必为K层
B.只能是M层
C.只有是L层
D.可以是任意层
参考答案:B
本题解析:
本题难度:简单