1��ѡ���� ������117��Ԫ��X��������������ȷ���ǣ�?��
A��X�����γ����Σ��仯ѧʽΪNaX
B��X������������ˮ������ǿ��
C��X�����������Ļ�ѧʽΪX2O7
D��X�ĵ���Ϊ˫ԭ�ӷ���
�ο��𰸣�C
�����������
�����Ѷȣ���
2��ѡ���� ����Ԫ��һ��������Ԫ�ص��ǣ�?��
A��ԭ�Ӻ���N���Ӳ���ֻ��һ�����ӵ�Ԫ��
B��ԭ�Ӻ���M�������Ϊż����Ԫ��
C��ԭ�Ӻ���M�������Ϊ������Ԫ��
D��ԭ�Ӻ���N�������Ϊ2��Ԫ��
�ο��𰸣�C
���������ԭ�Ӻ���N���Ӳ���ֻ��һ�����ӵ�Ԫ�ؿ���������Ԫ����K��Ҳ���ܲ�������Ԫ����Cu��Cr������A����ԭ�Ӻ���M�����Ϊż������M�����������Ϊ2��4��6��8������Ϊ0��Ԫ�أ���һ��������Ԫ�أ�����B������ԭ�Ӻ���M�������Ϊ������˵����Ԫ��ԭ�ӵ�M�㼴Ϊ����㣬�����������Ϊ1��3��5��7������������������������������C��ȷ��ԭ�Ӻ���N�������Ϊ2��Ԫ�ؿ���������Ԫ����Ca��Ҳ���ܲ�������Ԫ����Zn������D����
�����Ѷȣ�һ��
3��ѡ���� ���н����Ǵ�ijͬѧ����ҵ����ժ¼�ģ���������Ϊ�϶���ȷ����
�����뾶��S2->Cl->Cl>S ?���⻯���ȶ��ԣ�HF>HCl>H2S>H2Se
�ۻ�ԭ�ԣ�S2->Cl->Br->I-?�������ԣ�Cl2>S>Se
�����ԣ�H2SO4>HClO4>H2SeO4 �õ���������F>Cl>Br>I
A��ֻ�Т�
B���ڢܢ�
C���٢ۢ�
D��ֻ�Т�
�ο��𰸣�B
�������������Ԫ�������ɿ�֪���ٲ���ȷ�����뾶Ӧ����S2->Cl- >S>Cl���ǽ�����Խǿ���⻯����ȶ���Խǿ������ȷ���ǽ�����Խǿ����Ӧ�����ӵĻ�ԭ��Խ�����۲���ȷ����ԭ��Ӧ����S2->I->Br->Cl-���ǽ�����Խǿ����Ӧ���ʵ�������Խǿ������ȷ���ǽ�����Խǿ������������ˮ���������Խǿ���ݲ���ȷ��Ӧ����HClO4>H2SO4> H2SeO4��ͬ�������϶��£��ǽ���������������ȷ����ѡB��
�����������Ǹ߿��еĸ�Ƶ�⣬�����е��Ѷȵ����⣬�����ۺ���ǿ����Ҫ�ǿ���ѧ����Ԫ�������ɵ���Ϥ�˽�̶ȣ��Լ��������Ԫ��������֪ʶ���ʵ�������е�����������������ѧ�������������������ѧ����Ӧ��������ѧϰЧ�ʡ�
�����Ѷȣ�һ��
4��ѡ���� ϡ�����л����������ᣬΪ�˳�ȥ���ᣬ�ɼ�������
A.��м
B.�Ȼ�����Һ
C.��������Һ
D.����������Һ
�ο��𰸣�B
������������������ݳ����ʵ�ԭ�����ȷ���Ҫ���У���Ҫ�ܳ������ʣ��ֲ��ܺ���Ҫ�����ʷ�Ӧ��ͬʱҲ���������µ����ʣ����⣬ʵ�����Խ��Խ�ã�Ҫ��ȥ�����е����ᣬʵ�ʾ��dz���������ӣ����ú������ӵ���Һ�������ת���ɳ�����ͬʱ�������ᣮ
���A����м�����ᡢ���ᶼ��Ӧ�����Σ�����������Ҳ�����ˣ��������µ����ʣ���A����
B���Ȼ����ܰ�����ת�������ᱵ������ͬʱ�õ����ᣬ��B��ȷ��
C���������ܺ����ᷴӦ��������Ҳ�����ˣ���C����
D������������ͬʱ�����ᡢ���ᷴӦ��������Ҳ�����ˣ���D����
��ѡB��
���������⿼���˳����Լ���ѡȡ���ѶȲ�����ѡ��������Լ�ʱ����ѡ�Լ����ܺ�ԭ���ʷ�Ӧ��ԭ���ʵ��������ܼ��٣��������ӣ��ݴ˷������ɣ�
�����Ѷȣ�һ��
5������� X��Y��Z��W��Ԫ�����ڱ�ǰ�����ڳ���������Ԫ�أ�ԭ��������������Xԭ�Ӻ�����������״�ĵ����ƣ�������չ����������˫ԭ�ӷ��Ӵ��ڣ������ȶ���Y�ĵ����������г����ĺϽ���ϳɷ�֮һ��ԭ�Ӻ���ֻ��һ��δ�ɶԵ��ӣ�Zԭ�ӵİ뾶��X�����̬ԭ��������p�����Ǹò�s���ӵ�������W������ĺ�ɫ����֮һ��
��1��Zλ��Ԫ�����ڱ��е�λ����?��W3+�����������Ų�ʽ��______��X��������XO2��H2O�Ƚϣ��۵�ϸߵ���______ (�ѧʽ)��
��2�����������£�Z�ĵ�����������X������������ˮ�����Ũ��Һ��Ӧ������Z�����{�ۺ����ᣬд���˷�Ӧ�Ļ�ѧ����ʽ?��.
��3���Ƚ�Y��W���ʵĻ�����?����һ����ѧ��Ӧ����ʽ��ʾ����
��4��2013�����ȫ�����ض�����ж�������ʮ������������ɡ������족����Ҫ��Դ֮һ������β����ȼúβ���ŷų����Ĺ���С����PM2.5������β����������Ҫԭ��Ϊ��2NO(g)+2CO(g) 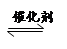 2CO2(g)+N2(g)�����ܱ������з����÷�Ӧʱ��c(CO2)���¶ȣ�T���������ı������S����ʱ�䣨t���ı仯������ͼ��ʾ��
2CO2(g)+N2(g)�����ܱ������з����÷�Ӧʱ��c(CO2)���¶ȣ�T���������ı������S����ʱ�䣨t���ı仯������ͼ��ʾ��
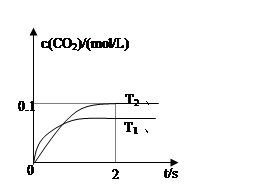
�ݴ��жϣ�
�÷�ӦΪ?��Ӧ�����ȡ����ȣ�����T2�¶��£�0~2s�ڵ�ƽ����Ӧ���ʣ���(N2)=?��
��5�����������������һ��ʱ�����������������ѧ��Ӧ���ʡ��������ı����S1��S2��
����ͼ�л���c(CO2)��T1��S2�����´ﵽƽ������еı仯���ߡ�
��6�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ�̴ﵽƽ��״̬����?������ţ���
����ͼ�Ц�����K��n��w�ֱ��ʾ����Ӧ���ʡ�ƽ�ⳣ�������ʵ�����������
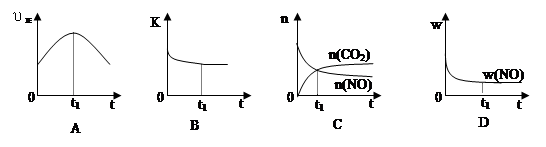
�ο��𰸣���1����������?��A��? 3s23p63d5? H2O
��2��S+6HNO3(Ũ) 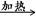 H2SO4+6NO2��+2H2O��
H2SO4+6NO2��+2H2O��
��3��Fe2O3 + 2Al 2Fe+Al2O3
2Fe+Al2O3
��4������? 0.025 mol/L��s
��5��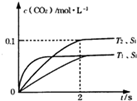
��6��B? D
�����������1��X��Y��Z��W��Ԫ�����ڱ�ǰ�����ڳ���������Ԫ�أ�ԭ��������������Xԭ�Ӻ�����������״�ĵ����ƣ�������չ����������˫ԭ�ӷ��Ӵ��ڣ������ȶ�����XΪN��Y�ĵ����������г����ĺϽ���ϳɷ�֮һ��ԭ�Ӻ���ֻ��һ��δ�ɶԵ��ӣ���YΪAl;Zԭ�ӵİ뾶��X�����̬ԭ��������p�����Ǹò�s���ӵ���������ZΪS��W������ĺ�ɫ����֮һ����WΪFe;���Ͽ�֪Zλ��Ԫ�����ڱ��е�λ���ǵ������ڢ�A�壬W3+�����������Ų�ʽ��3s23p63d5��X��������NO2��H2O�Ƚϣ��۵�ϸߵ���H2O��
��2����ѧ����ʽΪ��S+6HNO3(Ũ)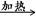 H2SO4+6NO2��+2H2O
H2SO4+6NO2��+2H2O
��3���û���Ӧ���Է�ӳ�����Ļ��ó̶ȣ���ѧ��Ӧ����ʽΪ��Fe2O3 + 2Al 2Fe+Al2O3
2Fe+Al2O3
��4����ͼ��֪���¶�T1�ȵ���ƽ�⣬���¶�T1��T2���¶�Խ��ƽ��ʱ��������̼��Ũ��Խ�ͣ�˵�������¶�ƽ�����淴Ӧ�ƶ���������ӦΪ���ȷ�Ӧ����ͼ��֪��T2�¶�ʱ2s����ƽ�⣬ƽ��ʱ������̼��Ũ�ȱ仯��Ϊ0.1mol/L����v��CO2��=0.1mol/L/2s=0.05mol/��L?s��������֮�ȵ��ڻ�ѧ������֮�ȣ���v��N2��=1/2v��CO2��=1/2��0.05mol/��L?s��=0.025mol/��L?s����
��5���Ӵ����Խ��Ӧ����Խ�죬����ƽ���ʱ��Խ�̣������ı����S1��S2��S2�����´ﵽƽ������ʱ���������������Ӱ��ƽ���ƶ���ƽ��ʱ������̼��Ũ�����¶�T1����ƽ��ʱ��ͬ����c��CO2����T1��S2�����´ﵽƽ������еı仯����Ϊ��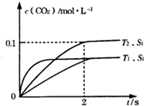 ��
��
��6��A������ƽ���������������ȣ����ٱ仯��t1ʱ��V�����֮���淴Ӧ�������ʷ����仯��δ����ƽ�⣬��A����B���÷�Ӧ����ӦΪ���ȷ�Ӧ���淴Ӧ�����¶����ߣ���ѧƽ�ⳣ����С������ƽ����¶�Ϊ��ֵ������ߣ�ƽ�ⳣ�����䣬Ϊ��С��ͼ����ʵ�ʷ��ϣ���B��ȷ��C��t1ʱ�̺������̼��NO�����ʵ��������仯��t1ʱ��δ����ƽ��״̬����C����D��NO����������Ϊ��ֵ��t1ʱ�̴���ƽ��״̬����D��ȷ��
�����Ѷȣ�����