1��ѡ����
��֪��Ȼ����ҿ�������������ֱ�Ϊ191��193��ͬλ�أ���ҿ��ƽ�����ԭ������Ϊ192.22��������ͬλ�ص�ԭ�Ӹ�����ӦΪ��?��
A��39��61
B��61��39
C��1��1
D��39��11
�ο��𰸣��𰸣�A
���������
����ƽ�����ԭ���������弴�ɼ��㣺
�ⷨ1?��ҿ������ͬλ��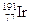 ��
��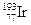 ��ԭ�����ֱ�Ϊ
��ԭ�����ֱ�Ϊ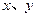 ��
��
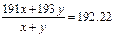 ?���
?���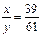
�ⷨ2
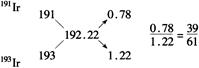
�����Ѷȣ�һ��
2��ѡ���� �±�Ϊ������Ԫ�آ�~��IJ������ʡ�
 Ԫ�ر�� Ԫ�ر��
Ԫ������
| ��
| ��
| ��
| ��
| ��
| ��
| ��
| ��
|
ԭ�Ӱ뾶/10-10m
| 0.66
| 1.36
| 1.23
| 1.10
| 0.99
| 1.54
| 0.70
| 1.18
|
����ϼ�
| ?
| +2
| +1
| +5
| +7
| +1
| +5
| +3
|
��ͻ��ϼ�
| ��2
| ?
| ?
| ��3
| ��1
| ?
| ��3
| ?
|
����˵����ȷ����?
A��Ԫ�آܢ��γɵĻ����������ӻ�����
B��Ԫ�آߵ���̬�⻯���ȶ��Ա�Ԫ�آܵ���̬�⻯���ȶ���ǿ
C��Ԫ�آ٢��γɵĻ������������
D���ϱ�8��Ԫ���У�Ԫ�آ۵�����������Ӧˮ����ļ�����ǿ
�ο��𰸣�
BC
�����������
�����Ѷȣ�һ��
3��ѡ���� ��֪����Ԫ�ص�ԭ�Ӱ뾶�����ݱ��������Ʋ���ԭ�ӵİ뾶������
ԭ��
| N
| S
| O
| Si
|
�뾶r/10-10m
| 0.75
| 1.02
| 0.74
| 1.17
|
A��0.80��10-10m? B��1.10��10-10m? C��1.20��10-10m? D��0.70��10-10m
�ο��𰸣�B
����������İ뾶�ڹ����֮�䣬1.02-------1.17,B��ȷ��
�����Ѷȣ���
4��ѡ���� ���ֶ�����Ԫ����Ԫ�����ڱ��е�λ������ͼ��ʾ������Z��ԭ�Ӱ뾶��С������˵����ȷ����
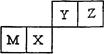
A��MԪ��һ��Ϊ����Ԫ��
B��XԪ�ص������̬�⻯������ȶ��Ա�ZԪ�صĴ�
C����YԪ�ش�����ۺ����ᣬ�����Ա�XԪ�ص���ۺ�������
D��ZԪ������Ԫ��һ�����γ�ԭ�Ӹ�����Ϊ1�U1�Ĺ��ۻ�����
�ο��𰸣�D
���������A.��Z��F����Y��O��X��P��M��Si��Si�Ƿǽ���Ԫ�ء�����B.Ԫ�صķǽ�����Խǿ�����Ӧ���⻯���ȶ��Ծ�Խǿ����Ԫ�����ڱ���ͬһ���ڵ�Ԫ�أ������ң�Ԫ�صķǽ���������ǿ����ͬһ�����У����ϵ��£�Ԫ�صķǽ��������������Էǽ�����Z>X������Z���⻯���ȶ��Ա�X��ǿ������C.ͬ���ǽ�����Y>X��Ԫ�صķǽ�����Խǿ��������������Ӧ��ˮ���������Խǿ������YԪ�ص���ۺ���������Ա�XԪ�ص���ۺ�����ǿ������D.����Z�ķǽ�������ǿ��ΪF����������H�γ�ԭ�Ӹ�����Ϊ1�U1�Ļ�����HFΪ���ۻ������ǿ��
�����Ѷȣ�һ��
5������� �±�ΪԪ�����ڱ���һ���֣������Ԫ�آ٣����ڱ��е�λ�ã��û�ѧ����ش��������⣺
��
 ���� ����
| IA
| ?
| 0
|
1
| ��
| ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| ?
|
2
| ?
| ?
| ?
| ��
| ��
| ��
| ?
| ?
|
3
| ��
| ?
| ��
| ��
| ?
| ��
| ��
| ?
|
 ��1��9��Ԫ���У�ԭ�Ӱ뾶��С����?��
��1��9��Ԫ���У�ԭ�Ӱ뾶��С����?��
��2���ܡ��ݡ�������Ԫ���γɵļ������У����Ӱ뾶������?��
��3���ڡ��ۡ��ߵ���ۺ������������ǿ������˳����__________________��
��4��Ԫ�آ۵��⻯��ĵ���ʽΪ?�����⻯�ﳣ���º͢���⻯�����߷�Ӧ��ʵ��������?��������Ӧ�õ�һ���Σ�����?����������ӻۣ������������Һ�������Ӵ��ڵķ�����?
��5���ݺ͢���Ԫ�ؿ��γɻ�����û���������ʱ������ɫΪ?ɫ���õ���ʽ��ʾ�û�������γɹ���?��
��6��д���������������ݵ�����������Ӧˮ���ﷴӦ�����ӷ���ʽ?��
 ��7���ɱ�������Ԫ�ص�ԭ�Ӱ�1��1��ɵij���Һ̬�������ϡ��Һ�ױ����ֽ⣬��ʹ�õĴ���Ϊ____________������ţ���
��7���ɱ�������Ԫ�ص�ԭ�Ӱ�1��1��ɵij���Һ̬�������ϡ��Һ�ױ����ֽ⣬��ʹ�õĴ���Ϊ____________������ţ���
 ?A��MnO2 B��FeCl3 C��Na2SO3? D��KMnO4
?A��MnO2 B��FeCl3 C��Na2SO3? D��KMnO4
�ο��𰸣� ��1��H?��2��O2-?��3��HNO3��H2CO3��H2SIO3
��1��H?��2��O2-?��3��HNO3��H2CO3��H2SIO3
��4��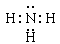 , �������̣����ӡ�ȡ�����ĸ�����Һ�����Թ��У�����Ũ��������������
, �������̣����ӡ�ȡ�����ĸ�����Һ�����Թ��У�����Ũ��������������
���ȣ���ʪ��ĺ�ɫ��ʯ����ֽ�������ɵ����壬��ֽ������˵������NH4+��
��5����ɫ�� 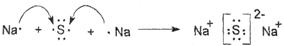
��6��Al2O3 + 2OH- ==2AlO2- + H2O ?��7��A B
?��7��A B
�������������Ԫ�������ڱ��е����λ�ÿ�֪��Ԫ�آ١���ֱ���H��C��N��O��Na��Al��Si��S��Cl��
��1��9��Ԫ���У�ԭ�Ӱ뾶��С����H��
��2����������Ų���ͬ�����������뾶��ԭ���������������С����ܡ��ݡ�������Ԫ���γɵļ������У����Ӱ뾶������O2-��
��3���ǽ�����Խǿ������������ˮ���������Խǿ�����Ԣڡ��ۡ��ߵ���ۺ������������ǿ������˳����HNO3��H2CO3��H2SIO3��
��4��Ԫ�آ۵��⻯���ǰ��������ڹ��ۻ���������ʽΪ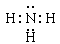 ���������Ȼ��ⷴӦ�������ӻ������Ȼ�泥������Dz������̡�NH4+����ķ�����ȡ�����ĸ�����Һ�����Թ��У�����Ũ�����������������ȣ���ʪ��ĺ�ɫ��ʯ����ֽ�������ɵ����壬��ֽ������˵������NH4+��
���������Ȼ��ⷴӦ�������ӻ������Ȼ�泥������Dz������̡�NH4+����ķ�����ȡ�����ĸ�����Һ�����Թ��У�����Ũ�����������������ȣ���ʪ��ĺ�ɫ��ʯ����ֽ�������ɵ����壬��ֽ������˵������NH4+��
��5���ݺ͢���Ԫ���γɻ����������ƣ��û���������ʱ������ɫΪ��ɫ�����γɹ�����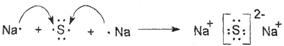 ��
��
��6��������������������������������ݵ�����������Ӧˮ���ﷴӦ�����ӷ���ʽ��Al2O3 + 2OH- ==2AlO2- + H2O ��
��
��7����������Ԫ�ص�ԭ�Ӱ�1��1��ɵij���Һ̬�������ϡ��Һ�ױ����ֽ⣬�û�����Ӧ����˫��ˮ�������ö������̺��Ȼ�������������ѡAB��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ�������������ѧ����������������Ӧ��������������Ҫ��Ԫ�ء�λ�������ԡ����߹�ϵ���ۺϿ��飬�Ƚ�ȫ�濼��ѧ���й�Ԫ���ƶ�֪ʶ���������֪ʶ��������������ѧ�������ʽṹ�����ʹ�ϵ�Լ�����Ԫ�������ɽ�����廯ѧ�����������
�����Ѷȣ�һ��