1、填空题 工业上对海水资源综合开发利用的部分工艺流程如下图所示。

(1)电解饱和食盐水常用离子膜电解槽和隔膜电解槽。离子膜和隔膜均允许通过的分子或离子是
________。电解槽中的阳极材料为__________。
(2)本工艺流程中先后制得Br2、CaSO4和Mg(OH)2,能否按Br2、Mg(OH)2、CaSO4顺序制备?
_____原因是_________________________。
(3)溴单质在四氧化碳中的溶解度比在水中大得多,四氧化碳与水不互溶,故可用于萃取溴,但在上述工艺中却不用四氯化碳,原因是____________________________。
参考答案:(1)阴离子(Na+);钛(或石墨)
(2)否;如果先沉淀Mg(OH)2,则沉淀中会夹杂有CaSO4沉淀,产品不纯
(3)四氯化碳萃取法工艺复杂、设备投资大,经济效益低、环境污染严重
本题解析:
本题难度:一般
2、填空题 工业上从海水中提取单质溴,其中一种工艺采用如下方法: ?
(1)向海水中通入Cl2,将海水中的溴化物氧化,其离子方程式为:___________________。 ?
(2)向上述混合物溶液中吹入热空气,将生成的溴吹出,用纯碱溶液吸收,这时,溴就转化成溴离子和溴酸根离子,其化学方程式为____________________________。 ?
(3)将(2)所得溶液用H2SO4酸化,又可得到单质溴,再用有机溶剂提取溴后,还可得到副产品Na2SO4。这一过程可用化学方程式表示为:______________________。 ?
(4)这样得到的溴中还混有少量Cl2,怎样除去?写出反应的离子方程式:______________________________。
参考答案:(1)Cl2+2Br-=Br2+2Cl-
(2)3Na2CO3+3Br2=5NaBr+NaBrO3+3CO2↑
(3)5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O
(4)Cl2+2Br-=Br2+2Cl-
本题解析:
本题难度:一般
3、选择题 提取食盐后的海水,又叫苦卤水,向里面加入Ca(OH)2 后,可以得到一种难溶于水的物质,这种物质再经过一系列的转化,最终可以得到
[? ]
A.Na
B.K
C.Mg
D.Ca
参考答案:C
本题解析:
本题难度:简单
4、选择题 海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案
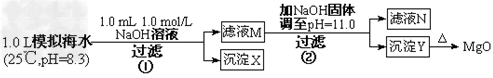
注:溶液中某种离子的浓度小于1.0×10-5?mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;Ksp[Ca(OH)2]=4.68×10-6;Ksp[Mg(OH)2]=5.61×10-12。下列说法正确的是
[? ]
A.沉淀物X为CaCO3
B.滤液M中存在Mg2+,不存在Ca2+
C.滤液N中存在Mg2+、Ca2+
D.步骤②中若改为加入4.2?g?NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
参考答案:A
本题解析:
本题难度:一般
5、填空题 海水中含有大量的氯化镁,从海水中提取镁的生产流程如图所示: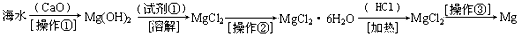
回答下列问题:
操作①主要是指______.试剂①可选用______,该反应的离子方程式为______.操作②是指______,经操作③最终可得金属镁,该反应的化学方程式是______.
参考答案:氢氧化镁是难溶性的固体,将不溶性的固体和溶液分离的方法是过滤,氢氧化镁和盐酸反应生成氯化镁和水,离子方程式为:Mg(OH)2+2H+=Mg 2++2H2O,从溶液中析出固体采用蒸发结晶的方法,镁是活泼金属,在工业上采用电解氯化镁的方法冶炼镁,其电解反应方程式为:MgCl2电解.Mg+Cl2↑,
故答案为:过滤,盐酸,Mg(OH)2+2H+=Mg 2++2H2O,蒸发结晶,MgCl2电解.Mg+Cl2↑.
本题解析:
本题难度:一般