1��ѡ���� ��������RԪ�ص�ԭ�ӣ�������ĵ�����Ϊ������������2������R��
A��Li
B��S
C��Si
D��P
�ο��𰸣�C
�������������ԭ�Ӻ�����ӵ��Ų����ɡ���������Ԫ�صĴ���㺬��8�����ӣ�����R��������������4����ԭ������Ϊ14����R�ǹ�Ԫ�ء���ѡC��
�����Ѷȣ�һ��
2��ѡ���� ���й��������ӵ�˵������ȷ����
A��ԭ�����ɷ��ӹ��ɵġ�
B��ԭ���к������ӡ����Ӻͺ�����ӡ�
C��ԭ����ʧȥ������ӣ�����������ӡ�
D��ԭ�����õ�������ӣ�����������ӡ�
�ο��𰸣�B
���������ԭ������ԭ�Ӻ˺ͺ�����ӹ��ɵģ���������ԭ�ӹ��ɵģ�A����ȷ��B��ȷ��ԭ����ʧȥ������ӣ�����������ӣ���֮ԭ�����õ�������ӣ�����������ӣ�CD���Ǵ���ģ���ѡB��
�����Ѷȣ���
3������� ��10�֣�������Ԫ��A��B��C��D�У�0.5mol AԪ�ص����ӵõ�6.02��1023�����ӱ���ԭΪ����ԭ�ӣ�0.4g A��������ǡ����100ml 0.2mol/L��������ȫ��Ӧ��Aԭ�Ӻ���������Ŀ��������Ŀ��ȣ�BԪ��ԭ�Ӻ�������������Ŀ�ȵ�һ���1����C�D��AԪ�ص����Ӷ�1�����Ӳ㣬DԪ�ص�ԭ�Ӻ���ڶ���ȵ�һ���2�����ӡ��ش��������⣺
(1)AԪ�ص�������_______��
��2��C�D�Ľṹʾ��ͼΪ?��DԪ�������ڱ��е�λ����__________��
��3��Ԫ��D����̬�⻯��ĵ���ʽΪ____������ӵĽṹ�ص��Ǿ���_____�ṹ����һ�������¸��⻯����뵥��C����ȡ����Ӧ�����������ʵ����ĸ��⻯���뵥��C��ϣ���һ�������³�ַ�Ӧ�������������ʵ���������_______���û�ѧʽ��д����
��4����ҵ��ұ������A�Ļ�ѧ����ʽΪ_____________________________________��
��5����ҵ�ϳ��õ���Bұ�����۵Ľ�����д���������͵���B�ڸ����·�Ӧ�Ļ�ѧ����ʽ_______������Ӧ����0.25mol�������μӷ�Ӧ��Ӧ��ת�Ƶ��ӵĸ���Ϊ__________��
��6����������A��B�õ������Ӳ��뵽����������Һ�п������ԭ��أ���������
����_______���û�ѧʽ��д���������缫��Ӧ��___________________________________��
�ο��𰸣�(1)þ? (2) 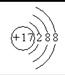 ���ڶ����ڡ���A? (3)
���ڶ����ڡ���A? (3)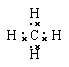 ����������? HCl?
����������? HCl?
(4) MgCl2(����)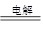 Mg��Cl2��?��5��Fe2O3��2Al
Mg��Cl2��?��5��Fe2O3��2Al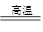 Al2O3��2Fe? 9.03��1023
Al2O3��2Fe? 9.03��1023
��6��Mg? 2Al��6e����8OH��=2AlO2����4H2O
�������������Ԫ�ص����ʺ������ڱ��е�λ�ÿ�֪��B����Ԫ�أ�D��̼Ԫ�ء�0.5mol AԪ�ص����ӵõ�6.02��1023�����ӱ���ԭΪ����ԭ�ӣ�˵��A������ǣ�2�ۡ�100ml 0.2mol/L��������0.02mol����������������ʵ�����0.01mol���Ҵ���Է���������40����A����������24. Aԭ�Ӻ���������Ŀ��������Ŀ��ȣ�����A��þ����C����Ԫ�ء�
��3�������Ǿ�����������ṹ���ӣ������ʽΪ �������к���4����ԭ�ӣ������������к����������Ȼ��⡣
�������к���4����ԭ�ӣ������������к����������Ȼ��⡣
��4��þ�ǻ��õĽ�����ͨ��������ڵ��Ȼ�þ����þ������ʽΪMgCl2(����)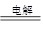 Mg��Cl2����
Mg��Cl2����
��5�����ǻ��õĽ������������ȷ�Ӧ�ķ���ʽΪFe2O3��2Al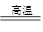 Al2O3��2Fe�������������Ļ��ϼ��ǣ�3�۵ģ�����0.25mol�������μӷ�Ӧת�Ƶĵ���Ϊ0.25mol��3��2��1.5mol���������Ϊ1.5mol��6.02��1023��9.03��1023��
Al2O3��2Fe�������������Ļ��ϼ��ǣ�3�۵ģ�����0.25mol�������μӷ�Ӧת�Ƶĵ���Ϊ0.25mol��3��2��1.5mol���������Ϊ1.5mol��6.02��1023��9.03��1023��
��6��������������������Һ��Ӧ������������������þ��������������ӦʽΪ2Al��6e����8OH��=2AlO2����4H2O��
�����Ѷȣ�һ��
4��ѡ���� ���и������Ӳ��ܻ���Ϊ�ȵ�������ǣ�?��
A��CO��N2
B��N2H4�� C2H4
C��CO2��N2O
D��O3��SO2
�ο��𰸣�B
���������A��CO��N2��ԭ�Ӹ�����Ϊ2���۵�������ǰ��̼Ϊ4����Ϊ6����Ϊ10�����ߵ�Ϊ5��2������Ϊ10��ԭ�����ͼ۵���������ȣ����ڵȵ����壬��A��ȷ��
B��N2H4��C2H4��ԭ�Ӹ�����Ϊ6���۵�������ǰ�ߵ�Ϊ5����Ϊ1����Ϊ14������̼Ϊ4����Ϊ1����Ϊ12��ԭ������ȣ����۵���������ȣ������ڵȵ����壬��B����
C��CO2��N2O��ԭ�Ӹ�����Ϊ3���۵�������ǰ��̼Ϊ4����Ϊ6����Ϊ16�����ߵ�Ϊ5����Ϊ6����Ϊ16��ԭ�����ͼ۵���������ȣ����ڵȵ����壬��C��ȷ��
D��O3��SO2��ԭ�Ӹ�����Ϊ3���۵�������ǰ����Ϊ6����Ϊ18�������������Ϊ6����Ϊ18��ԭ�����ͼ۵���������ȣ����ڵȵ����壬��D��ȷ��
��ѡB��
���������⿼���˵ȵ����壬�����ؼ��dz������ȵ�����ı����������Ѷ��еȡ�
�����Ѷȣ���
5��ѡ���� ��ѧ������2000�����Ӣ������Ȼ����־�ϱ��棬������DNA�������һ�ֱ۳�ֻ��7�����������ӣ��Ա��ܹ�ǯ����ӻ�ԭ�Ӳ�������������ϡ����з�ɢϵ�еķ�ɢ�ʵ�����ֱ�����������Ӿ�����ͬ����������
A.��Һ
B.����Һ
C.����Һ
D.����
�ο��𰸣�D
���������
�����Ѷȣ�����