1������� ��ѧѧϰС��Ϊ�ⶨ�����⡱��С��װ��Fe�ۺͻ���̿����֮�Ƚ���������̽����
�������ϣ������⡱��С��װ�����������ɷ�ΪFe�ۡ�����̿������NaCl��ˮ��
ʵ�鲽�裺
����һ��ȡijʳƷ��װ���еġ����⡱�ơ���������һ����������Ĺ��嵹����ֽ�ϣ���ϸ�۲죬����Ϊ�Һ�ɫ��ĩ��������һЩ����ɫ��ĩ��
�������������һ�еĹ�������ˮ�����ˣ�������ϴ�ӡ�����Գ�ȥ������������NaCl��ˮ��
��������ȡ������е������������Ϊ���ȷݣ�ÿһ������Ϊ16.0g��������һ�����������г�����գ����ɵ�����ȫ��ͨ�������ó���ʯ��ˮ���õ���������ij���20.0?g��
�����ģ����������е���һ�����������ձ��У�����һ�����������ϡH2SO4��������Ӧ��ȫ��
�����壺�����ĵĻ�����м������������������Һ�����˺�ù��壬��ϴ�Ӻ�ת�Ƶ������г�ּ��ȣ���ȴ���������õ�����������Ϊ16g��
��ش��������⣺
��1���ɲ���һ��֪�����������������еĺ���ɫ����Ϊ______���ѧʽ����
��2���ɲ�������֪��16.0?g�����л���̿������Ϊ______g��
��3������ʵ����֪���á�����������δ��������Fe�ۺͻ���̿����֮��Ϊ______��
��4���á����������У����ѱ������İٷ���Ϊ______��
�ο��𰸣���1���ڽ��������������У�ֻ���������Ǻ���ɫ�Ĺ��壬���ԡ����������еĺ���ɫ����ΪFe2O3���ʴ�Ϊ��Fe2O3��
��2���ɲ��������̼Ԫ���غ㣬�õ���������ij���20.0g��Ϊ̼��Ƶ�����������̼���ʵ�����Ϊx����
C��CO2��CaCO3��
12? 100
x? 20g
12x=10020g��
���x=2.4g������16.0g�����л���̿������Ϊ2.4g���ʴ�Ϊ��2.4g��
��3������ʵ�飬��������Լ��������Ļ�����м���һ�����������ϡH2SO4��������Ӧ��ȫ���ټ������������������Һ�����˺��ù���������������ϴ�Ӻ�ת�Ƶ������г�ּ��ȣ���ȴ���������õ���������������Ϊ16g��Ϊ0.1mol���������Ԫ���غ㣬������������ʵ���Ϊm�������������ʵ���Ϊn��
��
���������
�����Ѷȣ�һ��
2��ѡ���� ���з�Ӧ����������ԭ��Ӧ���ǣ�������
A��CuO+2HCl�TCuCl2+H2O
B��CaO+H2O�TCa��OH��2
C��CaCO3
CaO+CO2��
D��2KClO32KCl+3O2��
�ο��𰸣�A���÷�Ӧ��û��Ԫ�صĻ��ϼ۱仯��Ϊ��������ԭ��Ӧ����A��ѡ��
B���÷�Ӧ��û��Ԫ�صĻ��ϼ۱仯��Ϊ��������ԭ��Ӧ����B��ѡ��
C���÷�Ӧ��û��Ԫ�صĻ��ϼ۱仯��Ϊ��������ԭ��Ӧ����C��ѡ��
D����Ӧ�У�ClԪ�صĻ��ϼ۽��ͣ�OԪ�صĻ��ϼ����ߣ�����������ԭ��Ӧ����Dѡ��
��ѡD��
���������
�����Ѷȣ�һ��
3������� ƫ��������N2O4�dz��õĻ���ƽ��������߷������»�ѧ��Ӧ��
��CH3��2NNH2��l��+2N2O4��l���T2CO2��g��+3N2��g��+4H2O��g��������
��1����Ӧ��������������______��
��2������к��г��ֺ���ɫ���壬ԭ��Ϊ��N2O4��g��?2NO2��g��������
���¶�����ʱ��������ɫ�����Ӧ����Ϊ______������ȡ����ȡ�����Ӧ��
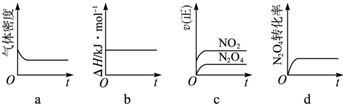
��3��һ���¶��£���Ӧ�����ʱ�Ϊ��H���ֽ�1mol?N2O4����һ��ѹ�ܱ������У�����ʾ��ͼ��ȷ����˵����Ӧ�ﵽƽ��״̬����______��������ͬ�¶��£�������Ӧ�������Ϊ1L�ĺ����ܱ������н��У�ƽ�ⳣ��______����������䡱��С��������Ӧ3s��NO2�����ʵ���Ϊ0.6mol����0��3s�ڵ�ƽ����Ӧ����v��N2O4��=______?mol/��L?s��-1��
��4��NO2���ð�ˮ��������NH4NO3��25��ʱ����a?mol?NH4NO3����ˮ����Һ�����ԣ�ԭ����______�������ӷ���ʽ��ʾ���������Һ�μ�b?L?��ˮ����Һ�����ԣ���μӰ�ˮ�Ĺ�����ˮ�ĵ���ƽ�⽫______������������������ƶ������μӰ�ˮ��Ũ��Ϊ______mol?L-1����NH3?H2O�ĵ���ƽ�ⳣ��ȡKb=2��10-5?mol?L-1��
�ο��𰸣���1����Ӧ��I���У�N2O4��l����NԪ�صõ��ӻ��ϼ۽��ͣ�����N2O4��l�������������ʴ�Ϊ����������
��2�������¶ȣ���ѧƽ�������ȷ�Ӧ�����ƶ������¶�����ʱ��������ɫ���ƽ��������Ӧ�����ƶ�����������Ӧ�����ȷ�Ӧ���ʴ�Ϊ�����ȣ�
��3��һ���¶��£���Ӧ�����ʱ�Ϊ��H���ֽ�1mol N2O4����һ��ѹ�ܱ������У�
a���ܶȵ����������������ƽ����ϵ�������䣬��Ӧ��������ܶ��ڷ�Ӧ�����в��䣬˵����Ӧ�ﵽƽ�⣬��a���ϣ�
b����Ӧ���ʱ�ͷ�Ӧ���������������ܺ�֮����㣬��ƽ���أ���b�����ϣ�
c��ͼ���Ʊ�ʾ����Ӧ���ʱ仯������֤�����淴Ӧ������ͬ����c�����ϣ�
d��N2O4��l��ת���ʲ��䣬֤����Ӧ�ﵽƽ�⣬��d���ϣ�
ʾ��ͼ��ȷ����˵����Ӧ�ﵽƽ��״̬����ad��K=c2(NO2)c(N2O4)����ѧƽ�ⳣ��ֻ���¶��йأ������ʵ�Ũ���أ�����ƽ�ⳣ��K���䣻v��NO2��=��c��t=0.6mol1L3s=0.2mol/L��s����v��N2O4��=12v��NO2��=0.1mol/L��s��
�ʴ�Ϊ��ad�����䣻0.1��
��4��NO2���ð�ˮ��������NH4NO3��25��ʱ����a mol NH4NO3����ˮ����Һ�����ԣ�����Ϊ笠�����ˮ�⣻��Ӧ�����ӷ���ʽΪ��NH4++H2O?NH3?H2O+H+�����백ˮ��Һ����笠�����ˮ�⣬ƽ��������У���a mol NH4NO3����ˮ�������Һ�μ�b L ��ˮ����Һ�����ԣ���Һ������������Ũ��=10-7mol/L��NH3?H2O�ĵ���ƽ�ⳣ��ȡKb=2��10-5 mol?L-1�����Ϻ���Һ���Ϊ1L������һˮ�ϰ�����ƽ��õ���NH3?H2O?NH4++OH-��ƽ�ⳣ��K=c(NH4+)c(OH-)c(NH3?H2O)=bmol/L��10-7mol/Lb��c(NH3?H2O)mol/L=2��10-5 mol?L-1������õ�c��NH3?H2O��=a200bmol/L��
�ʴ�Ϊ��NH4++H2O?NH3?H2O+H+������a200b��
���������
�����Ѷȣ�һ��
4������� ʵ���ҳ���ŨHCl��MnO2�ķ�Ӧ��ȡ�������������仯ѧ����ʽΪMnO2+4HCl=MnCl2+Cl2��+2H2Oȡһ������Ũ������������̷�����Ӧ�������������ڱ���µ����Ϊ11.2L����Ӧ�е�������Ϊ______���ѧʽ��������Ϊ______����ԭ��Ϊ______���ѧʽ�������ʵ���Ϊ______��ת�Ƶ��ӵ���ĿΪ______��
�ο��𰸣������������ڱ���µ����Ϊ11.2L�������ʵ���Ϊ11.2L22.4L/mol=0.5mol��
MnO2+4HCl=MnCl2+Cl2��+2H2O�У�MnԪ�صĻ��ϼ۽��ͣ���MnO2Ϊ����������MnO2��Cl2����֪��������Ϊ0.5mol��87g/mol=43.5g��
ClԪ�صĻ��ϼ����ߣ���HClΪ��ԭ������2HCl��Cl2����֪����ԭ�������ʵ���Ϊ0.5mol��2=1mol��
��Cl2����2e-��֪��ת�Ƶ�����Ŀ0.5mol��2��NA=NA����
�ʴ�Ϊ��MnO2��43.5g��HCl��1mol��NA��
���������
�����Ѷȣ�һ��
5��ѡ���� ���з�Ӧ�в�����������ԭ��Ӧ���ǣ�������
A��Cl2+2NaOH�TNaCl+NaClO+H2O
B��NH3+HCl�TNH4Cl
C��Br2+2KI�TI2+2KBr
D��2H2O2�T2H2O+O2��
�ο��𰸣�A��Cl2+2NaOH�TNaCl+NaClO+H2O��Ӧ�У�ClԪ�صĻ��ϼ۷����仯������������ԭ��Ӧ����A��ѡ��
B��NH3+HCl�TNH4Cl��Ӧ�У�����������Ԫ�صĻ��ϼ�û�з����仯��������������ԭ��Ӧ����Bѡ��
C��Br2+2KI�TI2+2KBr��Ӧ�У�Cl��BrԪ�صĻ��ϼ۷����仯������������ԭ��Ӧ����C��ѡ��
D��2H2O2�T2H2O+O2����Ӧ�У�OԪ�صĻ��ϼ۷����仯������������ԭ��Ӧ����D��ѡ��
��ѡB��
���������
�����Ѷȣ���