1、填空题 (13分)能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务。阅读下列有关能源的材料,回答有关问题:
(1)从能量的角度看,断开化学键要?,形成化学键要?。
(2)在生产和生活中经常遇到化学能与电能的相互转化。
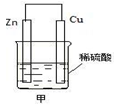
如图甲是将?能转化为?能的装置,负极电极反应式为?,发生______反应(填“氧化”或“还原”,下同)。正极现象?,发生______反应;发生反应时,电子由_____片流向_____片。当导线中有2 mol电子通过时,正极上析出?g 氢气。
参考答案:(1)吸收能量,释放能量。
(2)化学,电负极电极反应式为Zn-2e-=Zn2+,发生氧化反应,正极现象产生气泡,发生还原反应,锌片,铜片,2g
本题解析:锌铜原电池反应中,负极失去电子,经导线流向正极,被氧化:Zn-2e-=Zn2+;正极得电子,被还原:2H++2e-=H2↑;
本题难度:一般
2、填空题 (1)今有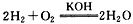 反应,构成燃料电池,则负极通入的应是_________,正极通入的应是
反应,构成燃料电池,则负极通入的应是_________,正极通入的应是
_______, 电极反应式为_____________;_____________。
(2)如把KOH改为稀H2SO4做电解质,则电极反应式为_____________;_____________。(1)和(2)的电池液不同,反应进行后,其溶液的pH各有何变化?______________________。
(3)如把H2改为甲烷,KOH做导电物质,则电极反应为_________________;_________________。
参考答案:(l)H2;O2;负极:2H2+4OH--4e-=4H2O;正极:O2+2H2O+4e-=4OH-
(2)负极:2H2-4e-=4H+;正极:O2+4H++4e-=2H2O;先变小,后变大
(3)负极:CH4+10OH--8e-=CO32-+7H2O;正极:2O2+4H2O+8e-=8OH-
本题解析:
本题难度:一般
3、选择题 据报道,某公司最近研制了一种由甲醇和氧气以及强碱作电解质溶液的新型手机电池,电量可达现用镍氢电池或锂电池的10倍,有关此电池的叙述,错误的是
[? ]
A.正极电极反应式:O2+2H2O+4e-=4OH -
B.负极电极反应式:CH3OH+6OH--6e-= CO2↑+5H2O
C.电池在使用过程中,电解质溶液的pH增大
D.当外电路通过1.2 mol电子时,理论上消耗甲醇6.4 g
参考答案:C
本题解析:
本题难度:一般
4、选择题 铜~锌原电池如图所示,电解质溶液为稀硫酸,下列说法不正确的是

A.铜电极上发生还原反应
B.锌电极是原电池的负极
C.电子从铜极经过外电路流向锌极
D.锌电极上的反应为Zn-2e― ="=" Zn2+