1������� ������Դ�Ŀ��������þ��й�����ǰ������ˮ��pHһ����7.5��8.6֮�䡣ij�غ�ˮ����Ҫ���ӵĺ������±���
�ɷ�
| Na��
| K��
| Ca2��
| Mg2��
| Cl��
| SO42-
| HCO3-
|
����/mg��L��1
| 9 360
| 83
| 200
| 1 100
| 16 000
| 1 200
| 118
|
?
��1�����������ǽ��귢չ������һ�ֽϺõĺ�ˮ������������ԭ������ͼ��ʾ��������(��)���ӽ���Ĥֻ������(��)����ͨ����
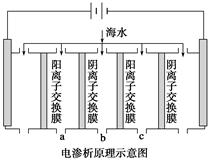
�������ĵ缫��ӦʽΪ__________________��
�ڵ��һ��ʱ�䣬�����������ˮ������ɷ�ΪCaCO3��Mg(OH)2��д������CaCO3�����ӷ���ʽ______________________________________��
�۵�ˮ�ij���Ϊa��b��c�е�________���ڡ�
��2����ˮ���Ԫ�ش����dz��ḻ���Ӻ�ˮ����ȡ﮵��о�����DZ����������컯ѧ��Դ����Ҫԭ�ϣ���LiFePO4���ij�缫�Ĺ���ԭ������ͼ��ʾ��
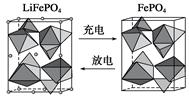
�õ�ص����Ϊ����Li���Ĺ�����ϡ��ŵ�ʱ�õ缫�ǵ�ص�________��(���������)���缫��ӦʽΪ______________________��
�ο��𰸣���1����2H2O��2e��=H2����2OH��
��Ca2����OH����HCO3-=CaCO3����H2O
��b
��2������FePO4��e����Li��=LiFePO4
�����������1���ٵ�⺣ˮ��������H���õ��ӣ������ǻ��ý��������ӣ�2H2O��2e��=H2����2OH����
��������������H�����Ϸŵ磬�ƻ�ˮ�ĵ���ƽ�⣬c(OH��)������ʹCa2����OH����HCO3-=CaCO3����H2O��
����Ϊ����������ȥCa2����Mg2�������Ե�ˮӦb�ڳ���
��2���ŵ�ʱ�ĵ缫��Ӧʽ�ֱ�Ϊ������Li��e��=Li����
������FePO4��Li����e��=LiFePO4��
�����Ѷȣ�һ��
2������� ��Դ�����ǵ�ǰ����������ٵ�һ���ش���⣬H2��CO��CH3OH������Ҫ����Դ���ʣ����ǵ�ȼ��������Ϊ285.8 kJ/mol��282.5 kJ/mol��726.7 kJ/mol����ش�
(1)��֪CO��H2��һ�������¿��Ժϳɼ״���CO+2H2=CH3OH����H2��CO��Ӧ����CH3OH���Ȼ�ѧ����ʽΪ�� ��
(2)��ͼΪij��ȼ�ϵ�صĹ���ԭ��ʾ��ͼ��a��b��Ϊ���Ե缫��

��ʹ��ʱ�������� ��ͨ��(�A����B��)��
�ڼ���ʹ�õġ�ȼ�ϡ��Ǽ״���a���ĵ缫��ӦʽΪ�� ________________
�ۼ���ʹ�õġ�ȼ�ϡ���ˮú��(�ɷ�ΪCO��H2)�����ֵ�ص��ͭ�����ƽ�������6.4 g�����������ı�״����ˮú�������Ϊ ��
�ο��𰸣�(1)CO(g)+2H2(g)=CH3OH(l) ��H="-127.4" kJ/mol
(2)��B
��CH3OH -6e-+8OH-=CO32-+6H2O
��2.24 L
���������(1)����������Ϣ����д��H2��CO��CH3OHȼ���ȵ��Ȼ�ѧ����ʽ��
(2)�ٴ�ͼ�Ͽ��Կ�����������a����b�����aΪ������bΪ����������Ӧ�ý�����������
��ע��״�ʧȥ���ӣ����ɵ�CO2Ҫ��OH-��Ӧת��ΪCO32-��
�۴��ƽ�������6.4 g��������0.1 mol Cu������ת��0.2 mol��������ˮú��0.1 mol����״�������Ϊ2.24 L
�����Ѷȣ�һ��
3��ѡ���� ��ͭ��п��ϡ������ɵ�ԭ����У����и�������ȷ����( )
A����Һ��pH�ɴ��С
B����Һ�е�SO42-��ԭ��ص������ƶ�
C��ZnΪ��صĸ������缫��Ӧ��Zn