1��ѡ���� ��ԭ�ӽṹʾ��ͼ�У�M��������Ŷ��ٵ��ӣ�
A.2
B.8
C.18
D.32
�ο��𰸣�C
�������������ԭ�ӵĺ�������Ų����ɣ�M���������2��32��18������ѡC��
�����Ѷȣ�����
2���ƶ��� ��A��B��C��D��E����Ԫ�أ����ǿ�����ԭ�ӻ����ӣ���Ϊ������Ԫ�أ�A��B���γ�BA�ͻ������AԪ���Ƿǽ�������ǿ��Ԫ�ء�����B��ԭ�Ӻ�������������ǰһ����ͬ����Ԫ��ԭ�ӵ���������8����CԪ��������ͬλ��C1��C2��C3����Ȼ���ﺬ��������C1��C3ԭ�ӵ���������C1��3����C2ԭ�ӵ���������C1��2����D����̬�⻯��ˮ��Һ�Լ��ԣ��������������ˮ����Ϊǿ�ᡣEԪ��ԭ�ӵ������������ȴ�����������4����E���ӵĺ������������������2����
��1��д��AԪ�����ƣ�____________��C2���ӵķ��ţ�___________��
��2������E���ӵĽṹʾ��ͼ��_______________��E���⻯��ķ���ʽ_______________��
��3��д��B��E���ϵĻ�ѧ����ʽ��________________________��
��4��д��A�ĵ��ʡ�B�ĵ��ʷֱ���ˮ��Ӧ����Һ��Ϻ����ķ�Ӧ�����ӷ���ʽ��____________________________________________��
��5��A��C�γɵĻ������к���ѧ�������ǣ�___________���õ���ʽ��ʾ�û�������γɹ��̣�_______________ ��?
�ο��𰸣���1������21H��2�� ��H2O
��H2O
��3��4Na+O2�T2Na2O ��2Na+O2 Na2O2
Na2O2
��4��HF+OH-��F-+H2O
��5�� ���ۼ������Լ�����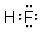
���������
�����Ѷȣ�һ��
3��ѡ���� ��(As)��ԭ�ӽṹΪ��������������ȷ����
A.��AsCl3�����У�As���������Ϊ8��
B.As���⻯��ΪAsH3����һ��ǿ������
C.As�����ԭ������Ϊ74.92���ɴ˿�֪As������Ϊ42
D.H3AsO4��ǿ��
�ο��𰸣�A
���������
�����Ѷȣ���
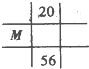
4��ѡ���� ���и�ͼΪԪ�����ڱ���һ���֣����е�����Ϊԭ������������MΪ37���ǣ�������
A��

B��

C��
D��
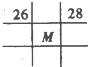
�ο��𰸣�M��ԭ������Ϊ37��λ�����ڱ��е������ڵڢ�A�壮
A��17�š�53��Ԫ��Ϊ�ڢ�A��Ԫ�أ�ͼ��MΪϡ������Kr����A����
B��19�ţ�55��Ԫ�ش��ڵڢ�A�壬MӦ���ڶ���֮�䣬��B����
C��20�ţ�56��Ԫ�ش��ڵڢ�A�壮20��Ԫ��Ϊ��Ԫ�أ����ڵ������ڵڢ�A�壬Mλ����ȷ����C��ȷ��
D��26�š�28��Ԫ��Ϊ�ڢ���Ԫ�أ�ͼ��M���ڵڢ��壬��D����
��ѡ��C��
���������
�����Ѷȣ���
5��ѡ���� ����Ԫ�����ڱ��еĹ��ɷ���������ƶϣ����д�����ǣ�������
A���루Be����һ�ֽ�������������������ˮ������ܾ�������
B������һ����ɫ���壬HAt���ȶ���AgAt����ɫ������ˮ�Ĺ���
C�������ȣ�SrSO4����������ˮ������İ�ɫ����
D�������⣨H2Se������ɫ���ж�����H2S�ȶ�������
�ο��𰸣�A��Be��Al�����ڱ���λ�ڶԽ���λ�ã��������ƣ����������������ԣ����루Be����һ�ֽ�������������������ˮ������ܾ������ԣ���A��ȷ��
B����±��Ԫ�ص��ʼ�������ĵݱ��Կ�֪�����ʵ���ɫ��ԭ��������������̬�⻯���ȶ��Լ�����±����������ˮ��������һ����ɫ���壬HAt���ȶ���AgAt����ɫ������ˮ�Ĺ��壬��B��ȷ��
C��Ca��Srλ��ͬ���壬�仯������������ƣ�����Ʋ�����ˮ�����ᣬ�������ȣ�SrSO4����������ˮ������İ�ɫ���壬��C��ȷ��
D��S��Seλ��ͬ���壬S�ķǽ����Դ���Se�������⣨H2Se������ɫ���ж����壬��H2S�ȶ��Բ��D����
��ѡD��
���������
�����Ѷȣ���