1��ʵ���� ��ҵ�Ͻ��������������ͨ�뵽���ʵ���Ũ��Ϊ0.375mol/LNaOH��Һ�еõ�Ưˮ��ijͬѧ����ʵ����̽��Cl2����
��ģ���Ʊ�Ưˮ����ͼ�Dz���ʵ��װ�á���֪KMnO4��������Һ��Ӧ������ȡCl2��

��1���������ʵ���Ũ��Ϊ0.375 mol/LNaOH��Һʱ����Ҫ�õ��IJ����������ձ�������������ͷ�ιܡ���Ͳ������������
��2��Ũ���������������������
��3��װ��E�з�����ѧ��Ӧ�����ӷ���ʽΪ����������
��4��װ��B�б���NaCl��Һ�����ڳ�ȥCl2�е�HCl���壬��֪������ˮ�ķ�Ӧ��һ�����淴Ӧ�����������NaCl��Һ��ȥCl2
��HCl�����ԭ���������ӷ���ʽ��ʾ������˵��������������
��5��ʵ��ʱװ��D��ʪ��ĺ�ɫֽ����ɫ�����ﲿ��û����ɫ������һ��ʱ���ֽ��ȫ����ɫ����ͬѧ��ΪCl2���ܶȱȿ�����
�������Թ��²�Cl2��Ũ�ȴ����Թ��ϲ�Cl2��Ũ�������µġ����жϸý����Ƿ��������������������ʵ�������ԭ������������
����Ľ����������Ʒ�����������������Ϊ����������ʿɲ��𣩡�
�ο��𰸣���12�֣���1������ƿ?��2����������
��3��Cl2 + 2OH�� = Cl�� + ClO�� + H2O
��4��HCl����ˮ�������H?+�ͱ���NaCl��Һ�е�Cl������Է�ӦCl2 + H2O 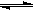 ��H?+ + Cl��+ HClO ����������
��H?+ + Cl��+ HClO ����������
��5����������ʵ�������Cl2��ʪ���ɫֽ���е�ˮ��Ӧ����HClOʹʪ��ĺ�ɫֽ����ɫ�����ﲿ��û��HClO������ֽ������ɫ������һ��ʱ�䣬����ˮ�����˶��ᵼ������ֽ��ʪ�����ɫ��
ȡһ���ϰ彫����ĺ�ɫֽ����ʪ��ĺ�ɫֽ���ֱ��������ϰ����࣬����װ�÷���װ��D�С���������ͨ��װ�и���ĺ�ɫֽ�����Թܣ���ͨ��װ��ʪ��ĺ�ɫֽ�����Թ��С�
���������ʵ��Ŀ�������������������������ʡ�Cl2(HCl/H2O)�����Ȼ�����Һ���������е��Ȼ������壬Ũ�������������ʹֽ����ɫ���Ǵ����ᣬ����������
�����Ѷȣ�һ��
2��ʵ���� ijͬѧΪ���о���������������µ�ʵ�飺
��1����һ�ձ��м���һ������ˮ����������ͭ����ɱ�����Һ
��2���ټ���һ����������ͭ
��3��ȡһС������ͭ���壬ȥ�������һС��
��4����ͷ��ϵס���壬����һͷϵ��һ�������ϣ��������ձ��ڣ������û����Һ��
��5����һҹ��ȡ������С���峤����
��ش���������
��1��ΪʲôҪ�ӹ���������ͭ���������������������Σ�___________________________________________________
��2��С���峤����˵��ʲô��____________________________________________
�ο��𰸣���1���ӹ���������ͭ��ʹ���峤����Ĵ�С���䣬���DZ����
��2��˵������Ĺ������Ρ�����ĸ�������
���������
�����Ѷȣ�һ��
3��ʵ����
|
��ջش�
ijͬѧΪ̽��ͭ��Ũ����ķ�Ӧ���������ͼ��ʾװ���Ƚ������й�ʵ��
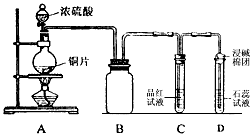
��1��B�������ռ�ʵ�������ɵ������װ�ã���δ�����ܻ�ȫ����ֱ����ԭͼ�ϰѵ��ܲ���������
��2����д��ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ��_______________________________��
��3��ʵ���У� C�е�����Ϊ________________��������Ϊ__________________��D�е�����Ϊ_________��������Ϊ________________��A�е���Һ������ɫ��Ϊ_________ɫ��
��4��ʵ���У���ͬѧȡ6.4gͭƬ��12mL 18mol/L H2SO4��Һ��Ũ������Բ����ƿ�й��ȣ�ֱ����Ӧֹͣ���������ƿ�л���ͭƬʣ�ࣻ��ͬѧ������ѧ�Ļ�ѧ֪ʶ�жϻ�����һ����H2SO4��ʣ�࣬����ж�����ȷ�ġ�
A��Ϊʲô����һ����H2SO4��ʣ�ࣿ________________________��
B�� ����ҩƷ���ܹ�������֤��Ӧֹͣ�����ƿ��ȷ��ʣ���H2SO4����_____________������ĸ��ţ�
a��BaCl2��Һ b��Ba(NO3)2��Һ c������ d��Na2CO3��ĩ
C��Ϊ�ⶨ�����H2SO4���ʵ�����ȡ����ʣ���ͭƬ��ϴ�ӡ���������Ϊmg�����ͨ������õ���
ʣ���H2SO4�����ʵ���=_____________mol��
��5������16gͭ��50mL H2SO4�����ʵ���Ũ��Ϊһ��ֵ��Ũ���ᷴӦ��ͭ��ȫ�ܽ⡣��ش�
�� ��Ӧ�в����������ڱ�״���µ����Ϊ____________L��
�� �÷�Ӧ�б���ԭ��H2SO4�����ʵ���Ϊ______________mol��
�� ������������ȫ���ͷź�����Һ�еμ�VmL a mol/L NaOH��Һ��ǡ��ʹ��Һ�е�Cu2+ȫ��ת��Ϊ��������ԭŨ������H2SO4�����ʵ���Ũ��=_____________mol/L��
�ο��𰸣���1�����ԡ�
��2��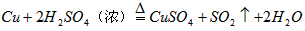
��3��Ʒ����Һ��ɫ������Ư�����ã���ɫʯ����Һ��죻��Ӧ�õ��ĵ���Һ�����ԣ���
��4��A����Ӧ������H2SO4���������ģ����ɵ�H2O�����࣬ʹŨ������ϡ��һ��Ũ�ȾͲ�����ͭ��Ӧ
B��d��C��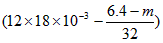
��5���� 5.6���� 0.25���� 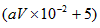
���������
�����Ѷȣ�����
4��ʵ���� ����22�֣�ijʵ��С��������װ�ý������µ�ʵ�顣?
��1��ʵ�������ͭ�����ֺ�ɫ�ͺ�ɫ�����������д����Ӧ�Ļ�ѧ����ʽ
?��?��
ʵ��С���ڲ��Ϲ������������£�Ϩ��ƾ��ƣ����ַ�Ӧ���ܼ������У�˵���÷�Ӧ��?��?����?��Ӧ��
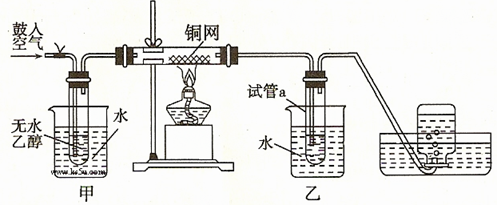
��2����������ˮԡ���ò���ͬ����������?��
�ҵ�������?��
��3����Ӧ����һ��ʱ������ԇ��a�����ռ�����ͬ�����ʣ���ô�ռ������л����ǣ�����д��ṹ��ʽ��?������ƿ���ռ��������������Ҫ�ɷ���?������д����ķ���ʽ��
��4�����Թ�a���ռ�����Һ������ɫʯ����ֽ���飬��ֽ�Ժ�ɫ��ʵ��С���ͬѧ��Ϊ������Ǵ��ڸ��������ᡣ��ȥ�����ʣ�����ʹ�ó����г�����һ�ֻ����������Ϊ? ������д��ѧʽ�����ʽ��
������д��ѧʽ�����ʽ��
��5����д������ʵ���漰���л����Ҵ������������е�һ�־���Ӧ�ã�?��
��6����ʵ���Ŀ���ǣ�?
�ο��𰸣���1����6�֣�2Cu+O2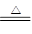 2CuO? CH3CH2OH+CuO
2CuO? CH3CH2OH+CuO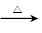 CH3CHO+Cu+H2O?���ȷ�Ӧ
CH3CHO+Cu+H2O?���ȷ�Ӧ
��2����4�֣�����?��ȴ?��3����6�֣���ȩ?�Ҵ�?����?
��4����2�֣�Na2CO3��NaHCO3?
��5����2�֣��磺�Ҵ����������ȣ���6����2�֣�̽���Ҵ�������ʵ��
��������������Ҵ�������ԭ��
��1����ɫ��ͭ����ɫ����ɫ������ͭ����ɫ��˵���ڼ��ȵ�������ͭ������������������ͭ������ͭ�ڼ��ȵ��������ֱ��Ҵ���ԭ������ͭ��Ϩ��ƾ��ƺ�Ӧ��Ȼ�ܽ��У�˵����Ӧ�Ƿ��ȷ�Ӧ���ų�����������ά�ַ�Ӧ�Ľ��С�
��2������װ�ÿ��жϣ����벣���ܵ����Ҵ����壬����ͨ������ʹ�Ҵ��ӷ��������Ҵ����塣��Ҫ�õ���������ȩ���ͱ��뽵���¶ȣ�ʹ��ȩҺ�����Һ�壬�����ռ���
��3����Ӧ�������еģ��������Ҵ��������������������ɵ���ȩһͬ����С�Թ��С��������еĵ���������ˮ���Ҳ����뷴Ӧ�����ռ�������ƿ�С�
��4����ֽ�Ժ�ɫ��˵����Һ�����ԣ���˵���ڷ�Ӧ���������������ɣ�����Ҫ��ȥ���ᣬ������̼�����ƻ�̼������Һ���ɡ�
��5��75���ľƾ���Һ����ԭ������������
��6������ʵ��ԭ����װ�ÿ�֪ʵ��Ŀ������̽���Ҵ�������ʵ��ġ�
�����Ѷȣ�һ��
5��ʵ���� �Ҷ����������ᣬij��ѧѧϰС���ͬѧ��̽���ⶨ���ᾧ�壨H2C2O4��xH2O����xֵ��ͨ���������ϸ�С��ͬѧͨ�������ѯ�ã�����������ˮ��ˮ��Һ����������KMnO4��Һ���еζ���2MnO4����5H2C2O4��6H��?2Mn2����10CO2����8H2O
����ͬѧ����˵ζ��ķ����ⶨxֵ��
�� ��ȡ1.260 g�����ᾧ�壬�������Ƴ�100.00 mLˮ��ҺΪ����Һ��
�� ȡ25.00 mL����Һ������ƿ�У��ټ���������ϡH2SO4
�� ��Ũ��Ϊ0.1000 mol/L��KMnO4����Һ���еζ����ﵽ�յ�ʱ����10.00 mL��
��ش�
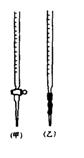
�� �ζ�ʱ����KMnO4��Һװ����ͼ�е�?����ס����ҡ����ζ����С�
�� ��ʵ��ζ��ﵽ�յ�ı�־������?��
�� ͨ���������ݣ������x=?��
���ۣ������ζ��յ�ʱ���ӵζ��̶ܿȣ����ɴ˲�õ�xֵ��?���ƫ����ƫС�����䡱����ͬ����
�����ζ�ʱ���õ�KMnO4��Һ����ö�����Ũ�ȱ�С�����ɴ˲�õ�xֵ��?��
�ο��𰸣���1���ף�2�����һ�θ�����ص�����ҺͻȻ������ɫ�����Ϻ�ɫ�����Ұ�����ڲ���ɫ��3��2?��ƫ�� ?��ƫС
�����������
�����Ѷȣ���