1、选择题 下列有关物质的用途错误的是( )
A.水玻璃可用作木材防火剂
B.二氧化硅是制造光导纤维的材料
C.石英是制造太阳能电池的常用材料
D.石灰石和纯碱均是生产普通玻璃的原料
参考答案:C
本题解析:
本题难度:简单
2、选择题 碳化硼陶瓷硬度大,熔点高,化学性质稳定.据此推出下列不能做为碳化硼陶瓷的用途的是( )
A.作耐磨材料
B.制作化学仪器(如坩埚)
C.作润滑材料
D.制作切削工具
参考答案:C
本题解析:
本题难度:简单
3、选择题 据报导,我国某些城市的酸雨严重,为改变这一状况,某市正准备推广使用的清洁能源,下列所列能源是清洁能源的是(?)
A.太阳能
B.石油
C.天然气
D.煤
参考答案:A
本题解析:酸雨的形成主要是化石燃料的燃烧,要改变这一现状,发展清洁能源,故答案为A。
本题难度:简单
4、填空题 (12分)以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如下表。
难溶物
| Ksp
|
Ca3(AsO4)2
| 6.8×10-19
|
AlAsO4
| 1.6×10-16
|
FeAsO4
| 5.7×10-21
|
表1.几种砷酸盐的Ksp?
污染物
| H2SO4
| As
|
浓度
| 28.42 g/L
| 1.6 g・L-1
|
排放标准
| pH 6~9
| 0.5 mg・L-1
|
表2.工厂污染物排放浓度及允许排放标准
回答以下问题:
⑴该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=______________mol・L-1。
⑵写出难溶物Ca3(AsO4)2的Ksp表达式:Ksp[Ca3(AsO4)2]=______________,若混合溶液
中Al3+、Fe3+的浓度均为1.0×10-4mol・L-1,c(AsO43-)的最大是_______________mol・L-1。
⑶工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式________________________________。
⑷在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH
调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为______________;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为_____________________________。
参考答案:12分)⑴0.29
⑵c3 (Ca2+)・c2 (AsO43-)? 5.7×10-17
⑶2H++MnO2+H3AsO3=H3AsO4+Mn2++H2O
⑷①CaSO4?
②H3AsO4是弱酸,当溶液中pH调节到8左右时AsO43-浓度增大,Ca3(AsO4)2开始沉淀
(每空2分,共12分)
本题解析:
(1)图表中硫酸浓度为28.42g/L,换算物质的量浓度=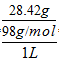 =0.29mol/L
=0.29mol/L
(2)难溶物Ca3(AsO4)2的沉淀溶解平衡为:Ca3(AsO4)2(s)?3Ca2++2AsO43-;溶度积Ksp=c3(Ca2+)?c2?(AsO43-);若混合溶液中Al3+、Fe3+的浓度均为1.0×10-4mol?L-1,依据Ksp大小可以得到,Ksp(FeAsO4?)小,反应过程中Fe3+先析出沉淀;依据Ksp(FeAsO4?)=c(Fe3+)c(AsO43-)=5.7×10-21;Fe3+的浓度均为1.0×10-4mol?L-1,计算得到?c(AsO43-)=5.7×10-17mol/L;
答案为:c3(Ca2+)?c2?(AsO43-);5.7×10-17;
⑶离子方程式2H++MnO2+H3AsO3=H3AsO4+Mn2++H2O
⑷①CaO+H2SO4=CaSO4+H2O,CaSO4是微溶,饱和而析出,答案:CaSO4?
②H3AsO4是弱酸,酸性条件下以主要以分子形式存在,随pH增大,AsO43-浓度增大,当溶液中pH调节到8左右时AsO43-浓度增大到Ca3(AsO4)2的浓度熵大于Ca3(AsO4)2的?Ksp Ca3(AsO4)2开始沉淀;
答案:H3AsO4是弱酸,当溶液中pH调节到8左右时AsO43-浓度增大,Ca3(AsO4)2开始沉淀。
本题难度:一般
5、选择题 下列各组金属最适合用H2或CO把它从化合物中还原出来的是
A.Ca、Mg
B.Al、Fe
C.Fe、Cu
D.Hg、Ag
参考答案:C
本题解析:考查金属的冶炼。活泼都金属通过电解法冶炼。不活泼的金属,通过热分解冶炼。处于中间的金属一般用还原剂还原,Ca、Mg、Al用电解法,D用热分解法,所以答案选C。
本题难度:简单