1������� ��12�֣��ڷ�ӦSO2 + Cl2 + 2H2O =" 2HCl" + H2SO4��,��������:______��
��ԭ����:_______________,��������������:________,������ԭ��Ӧ��������:___________.����1mol��HCl����ʱ,��Ӧ��ת�Ƶĵ�������:__________mol,�μӷ�Ӧ��SO2������_________��.
�ο��𰸣�(12��)��������:__ Cl2?____����ԭ����:_____ SO2________,
��������������:___ SO2____,������ԭ��Ӧ��������:___ Cl2_____.
��Ӧ��ת�Ƶĵ�������:____1_____ mol, SO2������____32_____��.
�����������
�����Ѷȣ�һ��
2��ѡ���� ��a g��ͭƬͶ��������һ��Ũ�ȵ�������Һ�У���Ӧ�����ĵ�HNO3Ϊb g����a��b��8��21����Ӧ�����������õ����������Ϊ(����)��
�ο��𰸣�D
���������agͭ��a/64mol������������ͭ��a/64mol�����Է�Ӧ�����������õ������������a/64mol��2��63g/mol��63a/32g������Ϊa��b��8��21��63a/32g��3b/4g����ѡD��
�����Ѷȣ�һ��
3��ѡ����  ��һ��Ũ�ȵ�
��һ��Ũ�ȵ�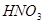 ��Ӧ������
��Ӧ������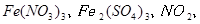

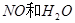 ����
����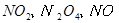 �����ʵ���֮��Ϊ
�����ʵ���֮��Ϊ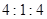 ʱ��ʵ�ʲμӷ�Ӧ��
ʱ��ʵ�ʲμӷ�Ӧ�� ��
��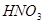 �����ʵ���֮��Ϊ��?����
�����ʵ���֮��Ϊ��?����
A��1:6
B��2:15
C��2:3
D��16:25
�ο��𰸣�A
��������� ��μӷ�Ӧ��FeSΪ1mol������Һ��Fe2��SO4��3Ϊ1/3mol��Fe��NO3��3Ϊ1/3mol����Ӧ��FeԪ�ء�SԪ�ػ��ϼ����ߣ�NԪ�ػ��ϼ۽��ͣ���NO2��N2O4��NO�����ʵ����ֱ�Ϊ4amol��amol��4amol�����ݵ���ת���غ��У�1����3-2��+1��[6-��-2��]=4a����5-4��+a����5-4����2+4a����5-2�������a=0.5����NO2��N2O4��NO�����ʵ����ֱ�Ϊ2mol��0.5mol��2mol���������������õ�HNO3Ϊ2mol+0.5mol��2+2mol=5mol����������õ���������Fe��NO3��3������������õ�����Ϊ1/3mol��3=1mol���μӷ�Ӧ������Ϊ5mol+1mol=6mol����ʵ�ʲμӷ�Ӧ��FeS��HNO3�����ʵ���֮��Ϊ1mol��6mol=1��6����ѡA��
�����Ѷȣ�һ��
4������� ��1���������ƺ͵������������Һ�з������·�Ӧ��
______Na2SO3+______KIO3+______H2SO4--______Na2SO4+______K2SO4+______I2+______H2O
����ƽ�����������ԭ��Ӧ����ʽ������ѧ���������뷽���У�
��������������______��
������Ӧ����5mol����ת�ƣ������ɵ�����ʵ�����______mol
��2����ɱ����е����ݣ�
| �ı������ | ƽ���ƶ��ķ��� | ƽ���ƶ��Ĺ���
����Ӧ���Ũ��
______
��Ӧ���Ũ��______
��Сѹǿ
______
��ϵ��ѹǿ��______
�����¶�
______
��ϵ���¶���______
ʹ�ú��ʵĴ���
______
����______
��ƽ������ʱ��______
|
��3����������ԭ��������ı�Ӱ��ƽ���һ����������Ũ�ȡ��¶ȡ�ѹǿ�ȣ���ƽ��������ܹ�______�ķ����ƶ���
�ο��𰸣���1���ٷ�Ӧ��SԪ�ػ��ϼ���Na2SO3��+4������Ϊ+6�ۣ��ܹ�����2�ۣ�IԪ�ػ��ϼ���KIO3��+5����ΪI2��0�ۣ��ܹ�����10�ۣ����ϼ���С������Ϊ10����Na2SO3ϵ��Ϊ5����I2ϵ��Ϊ1���ٽ��ԭ���غ���ƽ��ʽΪ5Na2SO3+2KIO3+H2SO4�T5Na2SO4+K2SO4+I2+H2O��
�ʴ�Ϊ��5��2��1��5��1��1��1��
�ڸ÷�Ӧ�У���Ԫ�صĻ��ϼ���+5�۱�Ϊ0�ۣ���Ԫ�صĻ��ϼ���+4�۱�Ϊ+6�ۣ�������������KIO3��
�ʴ�Ϊ��KIO3��
�۵�Ԫ�صĻ��ϼ���+5�۱�Ϊ0�ۣ�����1mol�ⵥ��ʱת��10mol���ӣ�����Ӧ����5mol����ת�ƣ������ɵĵ�����ʵ���=5mol10=0.5mol��
�ʴ�Ϊ��0.5��
��2������Ӧ���Ũ�ȣ�ƽ�������ƶ���ƽ���ƶ��Ĺ��̷�Ӧ���Ũ�ȼ�С����Сѹǿ��ƽ������������������ƶ���ƽ���ƶ��Ĺ�����ϵ��ѹǿ�����������¶ȣ�ƽ�������ȷ����ƶ���ƽ���ƶ��Ĺ�����ϵ���¶����ͣ�ʹ�ú��ʵĴ�����ƽ�ⲻ�ƶ������ʼӿ죬��ƽ������ʱ�����̣�
�ʴ�Ϊ��
�ı������ƽ���ƶ��ķ���ƽ���ƶ��Ĺ�������Ӧ���Ũ�������ƶ���Ӧ���Ũ�ȼ�С��Сѹǿ����������������ƶ���ϵ��ѹǿ�����������¶������ȷ����ƶ���ϵ���¶�����ʹ�ú��ʵĴ���ƽ�ⲻ�ƶ����ʼӿ�
��ƽ������ʱ�����̣�3����������ԭ��������ı�Ӱ��ƽ���һ����������Ũ�ȡ��¶ȡ�ѹǿ�ȣ���ƽ��������ܹ��������ָı�ķ����ƶ���
�ʴ�Ϊ���������ָı䣮
���������
�����Ѷȣ�һ��
5��ѡ���� ij�������ʸ�һ��Ũ�ȵ����ᷴӦ���ٶ�ֻ������һ�Ļ�ԭ������μӷ�Ӧ�ĵ����뱻��ԭ����������ʵ���֮��Ϊ2��1ʱ����ԭ�����ǣ�?��
A��NO2
B��NO
C��N2O
D��N2
�ο��𰸣�C
����������跴Ӧ��������ϼ�Ϊ+x����Ӧ��N���ϼ�Ϊ+y���ɵ�ʧ������ȵã�2x=5��y���������ϼ�һ��Ϊ+1��+2��+3������y�ֱ�Ϊ3��1����1��
������������ԭ����һ��Ҫץס��ʧ������ȡ�
�����Ѷȣ�һ��