1������� �ó������ⶨNaHCO3��K2CO3��������ɣ�ʵ�������ÿ�γ�ȡһ����������Ʒ����ˮ�Ƴ���Һ�������еμ���ͬŨ�ȵ�
Ba��OH��2��Һ��ÿ��ʵ�����ַ�Ӧ��ʵ���¼���±���
| ʵ����� | ��ȡ��Ʒ������/g | ����Ba��OH��2��Һ�����/L | ������ɳ�������/g
1
0.858
0.5
1.379
2
1.716
0.5
______
3
2.574
0.5
4.137
4
3.432
0.5
5.516
5
4.290
0.5
5.516
6
5.148
0.5
5.516
|
�ش��������⣺
��1����2��ʵ���в���������������______��
��2��Ba��OH��2��Һ���ʵ���Ũ����______��
��3��ͨ������ȷ����Ʒ��NaHCO3��K2CO3�����ʵ���֮����______��
�ο��𰸣���1����3�Ρ���4�����ɳ���̼�ᱵ��������Ϊ5.516g��˵����Ʒ����Ϊ3.342gʱ�����������Ѿ���ȫ��Ӧ����1�Ρ���3����Ʒ�������ֱ�Ϊ0.858g��2.574g����1�Ρ���3�����ɳ���̼�ᱵ�����ֱ�Ϊ1.379g��4.137g����Ʒ������֮�ȵ������ɵij�������֮��Ϊ1��2��˵����3��ǡ����ȫ��Ӧ����2��ʵ������Ʒ��ȫ��Ӧ���������������Ϊmg����
1.716g��2.574g=mg��4.137g�����m=2.758���ʴ�Ϊ��2.758g��
��2��ʵ����ÿ�εμ���ͬŨ�ȵ�Ba��OH��2��Һ50.5L����5�Ρ���5�����ɳ���̼�ᱵ������Ϊ5.516g��˵����Ʒ����Ϊ3.342gʱ�����������Ѿ���ȫ��Ӧ��̼�ᱵ�����ʵ���Ϊ5.516g197g/mol=0.028mol�����ݱ������غ��֪���������������ʵ���Ϊ0.028mol������Ba��OH��2��Һ�����ʵ����ʵ���Ũ����0.028mol0.5L=0.056mol/L���ʴ�Ϊ��0.056mol/L��
��3����3��ʵ������Ʒ��ȫ��Ӧ����̼��������̼��ص����ʵ����ֱ�Ϊxmol��ymol����
���������
�����Ѷȣ�һ��
2��ѡ���� ����װ�û�����ܴﵽʵ��Ŀ�ĵ���
 ?
?  ?
?  ?
? 
[? ]
A���٢ڢۢ�
B���ڢۢ�
C���ۢ�
D���٢�
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3��ѡ���� ���з�Ӧ��ȡ����������е��ǣ�������
A��Zn+H2SO4��ϡ��=ZnSO4+H2��
B��CaCO3+H2SO4��ϡ�� CaSO4+H2O+CO2��
CaSO4+H2O+CO2��
C��Na2SO3+H2SO4�TNa2SO4+H2O+SO2��
D��MnO2+4HCl��ϡ�� MnCl2+Cl2��+2H2O
MnCl2+Cl2��+2H2O
�ο��𰸣�A
���������
�����Ѷȣ�һ��
4��ѡ���� ����ʵ�鷽��������������ǣ�������
A����Ũ��ˮ���𣺱���CCl4��������Һ������ϩ
B����ȥNO�л��е�����NO2���ɽ��������ͨ��ʢ��ˮ��ϴ��ƿ�������ſ������ռ�NO
C�����Ʊ����ᶡ����ʵ���У����õ��Ĵֲ�Ʒ����ˮϴ������NaOH��Һϴ��Ȼ���Һ���ɵõ����ᶡ���ľ�Ʒ
D��SO42-�ļ��飺����HNO3�ữ��BaCl2��Һ���۲��Ƿ��а�ɫ��������
�ο��𰸣�A
���������
�����Ѷȣ���
5��ѡ���� ����װ����ʾ��ʵ���ܴﵽʵ��Ŀ�ĵ���
[? ]
A���������еĵ�;ƾ� 
B������е㲻ͬ�����ֻ���Һ�� 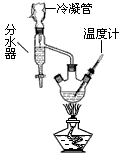
C����֤NH3���ܽ��� 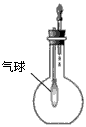
D���Ƚ�Na2CO3��NaHCO3�����ȶ��� 
�ο��𰸣�C
���������
�����Ѷȣ�һ��