1��ѡ���� ��������������ˮ�ֱ�μӵ�������Һ����ֽ�ϣ������۲쵽����������������һ���ǣ�������
| AgNO3��Һ | ��ɫʯ����ֽ | Na2CO3��Һ
A
��������
����������
������
B
����������
����������
��������
C
��������
�ȱ�����ɫ
������
D
��������
�ȱ�����ɫ
��������
|
A��A
B��B
C��C
D��D
�ο��𰸣�������ˮ������Cl2+H2O=HCl+HClO��HClO���������ԡ�ǿ�����ԡ�Ư�����Լ����ȶ��ԣ���ˮ�к���Cl2��HClO��H2O�ȷ��ӣ�����Cl-��H+��ClO-�����ӣ�
��ˮ�к��������ӣ����Ժ���������Һ��Ӧ���ɰ�ɫ������
��ˮ�к������ᡢ�����ᣬ��Һ�����ԣ�����ʹ��ɫʯ����ֽ��죬��������Ư���ԣ���ʹ����ʯ����ֽ��ɫ��
��ˮ�к������ᣬ�ܺ�̼������Һ��Ӧ���ɶ�����̼���壬���������ݲ�����
��ѡC��
���������
�����Ѷȣ���
2��ѡ���� ��������������벻����ѧ�����й��������еĻ�ѧ֪ʶ˵��������ǣ�������
A����������ʯ���鷴Ӧ���Ƶ�Ư��
B�������£��������۳�װ��Ũ����
C��������̼�������������γ��������Ҫԭ��
D������Ҫͨ����ѧ��Ӧ���ܴӺ�ˮ�л��ʳ�κ͵�ˮ
�ο��𰸣�A��������ʯ���鷴Ӧ�����Ȼ��ơ�������ƣ�ΪƯ�۵���Ҫ�ɷ֣���A��ȷ��
B��Ũ�������������ۻ���Ӧ���������۳�װ��Ũ���ᣬ��B��ȷ��
C�������������Ҫ��Ⱦ��Ϊ��������͵������������̼Ϊ����ЧӦ����Ҫ��Ⱦ���C����
D����������ķ����Ӻ�ˮ�л��ʳ�κ͵�ˮ��Ϊ�����仯����D��ȷ��
��ѡC��
���������
�����Ѷȣ���
3��ѡ���� ����˵������ȷ����?
A���ơ�����ͭһ��������������ȼ�����ɽ����Ȼ���
B�������������Ƿ�����Ȼ������壬������������Һ
C����������۽�����Ӧ���ɸ۽����Ȼ���
D����ˮ����ɱ����Ư������������ˮ�к���ǿ�����ԵĴ�����
�ο��𰸣�B
���������A���ơ�����ͭһ��������������ȼ�����ɽ����Ȼ��A��ȷ��B����������Һ��������ӦҲ���ɰ�ɫ�����Ȼ��������ܼ����������Ƿ�����Ȼ��⣬B����ȷ��C�����������������ԣ���������۽�����Ӧ���ɸ۽����Ȼ��C��ȷ����ˮ����ɱ����Ư������������ˮ�к���ǿ�����ԵĴ����ᣬD��ȷ����ѡB��
�����������Ǹ߿��еij������㣬��Ҫ�ǿ���ѧ�����������ʵ���Ϥ�˽�̶ȣ��ر�������Ư���ԣ������ڵ���ѧ����ѧϰ��Ȥ����ǿѧ����ѧϰ�����ģ�ע��ƽʱ֪ʶ�Ļ��ۺ�������
�����Ѷȣ�һ��
4������� �о���ѧϰС��������ϵ�֪��Ư�������ᷴӦ�����Ƶ���������ѧ����ʽΪ��Ca��ClO��2+CaCl2+2H2SO4
2CaSO4+2Cl2��+2H2O�����������������ȡ��������֤�����ʵ�ʵ�飮
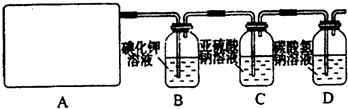
�Իش𣺣�1����ʵ����A���ֵ�װ����______����дװ�õ���ţ���
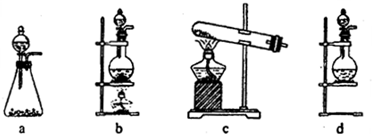
��2����1��ѡ����dװ�õ�������Ҫ�IJ�����������Ʒֱ���______��______��
��3���������һ��ʵ�飬֤��ϴ��ƿC�е�Na2SO3�Ѿ�������������ʵ�鲽�裩��______��
��4���ֱ�д��Cװ�á�Dװ�÷�����Ӧ�����ӷ���ʽ______��
��5����ʵ��������Ե�ȱ�ݣ�����ӻ�ѧ��Ӧ���ӽ�����Ľ��ķ�����______����������Ӧ�Ļ�ѧ����ʽ��______��
��6����С���ֽ���������ʵ�飺��ȡƯ��2.0g����ĥ���ܽ⣬���Ƴ�250mL��Һ��ȡ25mL���뵽��ƿ�У��ټ��������KI��Һ������H2SO4��Һ�����ã�����ȫ��Ӧ����0.1mol/L��Na2S2O3��Һ������Һ�ζ���Ӧ���ɵĵ⣬��֪��Ӧ����ʽΪ��
2Na2S2O3+I2�TNa2S4O6+2NaI?��Ӧ���ʱ������ȥNa2S2O3?20.0mL�����Ư����Ca��ClO��2����������Ϊ______����������0.01%��
�ο��𰸣���1��A����������ȡCl2����������Cl2�����ɷ�Ӧ�ķ�Ӧ��״̬�ͷ�Ӧ�Ƿ���Ҫ����ѡ�����巢��װ�ã�Ӧѡ���ڡ���+Һ?��?.?�����͵�b���ʴ�Ϊ��b��
��2��dװ�õ�������Ҫ�IJ�������ΪԲ����ƿ�ͷ�Һ©�����ʴ�Ϊ����Һ©����Բ����ƿ��
��3��Na2SO3�����IJ���ΪNa2SO4��ȷ������SO42-����֤��Na2SO3�Ѳ��ֱ�����������ʱ��ӦȡC����Һ�����ڽྻ�Թ��У��ȼ�ϡHCl�����ٲ����������ų�SO32-�ĸ��ţ�Ȼ���ټ���BaCl2��Һ����������ɫ��������֤��Na2SO3�Ѳ��ֱ�������
�ʴ�Ϊ��ȡ������Һ���ڽྻ���Թ��У������еμ�ϡ���������ٲ������壬�������е����Ȼ�����Һ����������ɫ������֤���������Ʊ�������
��4��Cװ����������ͨ������������Һ�з����ķ�Ӧ���������ƾ��л�ԭ�Ա���������Ϊ�����ƣ���Ӧ�����ַ���ʽΪ��Cl2+H2O+SO32��=SO42��+2Cl��+2H+������D��Cl2��ˮ��Ӧ�����ӷ���ʽΪCl2+H2O?H++Cl-+HClO��HCl����NaHCO3��Ӧ�����ӷ���ʽΪH++HCO3-=CO2��+H2O��HClO�����Ա�H2CO3����������NaHCO3��Ӧ��Cl2+H2O�TH++Cl-+HClO��H++HCO3-�TCO2��+H2O����HCO3��+Cl2=HClO+CO2��+Cl-��
�ʴ�Ϊ��Cl2+H2O+SO32��=SO42��+2Cl��+2H+��Cl2+H2O�TH++Cl-+HClO��H++HCO3-�TCO2��+H2O����HCO3��+Cl2=HClO+CO2��+Cl-��
��5��NaHCO3����Cl2���������ޣ���Dװ�ú�����һ��β������װ�ã�Ӧ��β��ͨ��NaOH��Һ�У���Ӧ�Ļ�ѧ����ʽΪ��Cl2+2NaOH=NaCl+NaClO+H2O��
�ʴ�Ϊ����Dװ�ú�����һ��β������װ�ã�Ӧ��β��ͨ��NaOH��Һ�У�Cl2+2NaOH=NaCl+NaClO+H2O��
��5����ϵʽCa��ClO��2��2Cl2��2I2��4Na2S2O3��
n[Ca��ClO��2]=14n��Na2S2O3��=20.0 mL��10-3 L?mL-1��0.1 mol?L-1��250ml25ml=0.005 mol��
Ca��ClO��2%=0.005mol��143g/mol2.0g��100%=35.75%��
�ʴ�Ϊ��35.75%��
���������
�����Ѷȣ�һ��
5������� ��11�֣��������ȼҵ����Ҫ��Ʒ֮һ����һ�ֳ��õ���������������ԭ������ˮ��Ӧ�����˴����
Cl2 + H2O  ?HCl + HClO?K=4.5��10-4
?HCl + HClO?K=4.5��10-4
�������ǿ��������ɱ��ˮ�еIJ�������ֱ���ô�����Ϊ����ˮ��������Ϊ�������ֽ⣬�Ҷ��Խϴ����ǣ������������˲����㣬�Ҿ���һ����Σ���ԣ�Ŀǰ��������������Խ��������Ʒ���������ش�
��1���ȼҵ���������Ļ�ѧ����ʽΪ?��
��2��ʹ������Ϊ����ˮ����������Ч �ؿ��ƴ������Ũ�ȣ�����ƽ�ⳣ������ԭ��?��
�ؿ��ƴ������Ũ�ȣ�����ƽ�ⳣ������ԭ��?��
��3��84����Һ��������Ⱦ������˷�����ŵ㣬���������ռ���Һ��Ӧ�Ʊ�84����Һ�����ӷ���ʽΪ?��
��4������������Ŀǰ�����Ϲ��ϵ�����һ���ĸ�Ч�����ס���ȫ��ɱ�������ʼ����ҹ���ѧ���з��������������������ƣ�NaClO2�������Ʊ��������ȵķ������仯ѧ����ʽΪ?��
��5��һλͬѧ�����һ����Ũ�����KMnO4������ȡ�����������Ƚ�������ⵥ�ʵ���
����ǿ������װ�ã���ͼ����
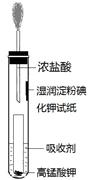
��������Һ������Cl2����?������ĸ��ţ���
A������ʳ��ˮ
B������Na2SO3��Һ
C������NaOH��Һ
D��Ũ����