1��ѡ���� ����п�̵�ص��ܷ�Ӧ�ǣ�Zn + 2MnO2 + 2H2O === 2MnOOH + Zn(OH)2���������KOH������˵����ȷ����
[? ]
A��MnO2������������Ӧ
B��MnOOH��MnԪ�صĻ��ϼ�Ϊ+3
C����Ӧ����0.65 g Zn����0.01 mol���ӷ���ת��
D����������ķ�ӦΪ��Zn + 2OH-- 2e-=== Zn(OH)2
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2��ѡ���� ���ھ��г��ͺĵ��������������ص㣬LED��ƷԽ��Խ���˻�ӭ����ͼ������ȼ�ϵ������LED�����װ�ã������й�������ȷ���ǣ�������

A��a��ͨ��������b��ͨ������
B����װ����ֻ�漰������ʽ������ת��
C����������缫��ӦʽΪO2+2H2O+4e-�T4OH-
D��Pһ�Ͱ뵼�����ӵ��ǵ�ظ���
�ο��𰸣�A���ɵ��������֪aΪ������bΪ�����������Ϸ���������Ӧ��ͨ�������������Ϸ�����ԭ��Ӧ��ͨ�������������A����
B����װ�õ�����ת���л�ѧ�ܡ����ܺ��ܣ���B����
C��aΪ�����������ĵ缫��ӦΪH2-2e-+2OH-�T2H2O��bΪ���������ĵ缫��ӦΪO2+2H2O+4e-�T4OH-����C��ȷ��
D��Pһ�Ͱ뵼�����ӵ��ǵ����������D����
��ѡC��
���������
�����Ѷȣ�һ��
3��ѡ���� ��ѧ�ҳɹ�������Яʽ����������ȼ�ϵ�أ����Ա�������Ϊȼ�ϣ�����е�һ��ͨ���������һ��ͨ��������壬������ǹ�̬�����������״̬���ܴ���O2-�����жԸ�ȼ�ϵ�ص�˵������ȷ���ǣ�������
A�������ڵ�����У�O2-�ɸ�����������
B���õ�ص��ܷ�Ӧ�ǣ�C3H8+5O2=3CO2+4H2O
C����·��ÿͨ��5mol���ӣ�Լ��5.6L��״���µı��鱻��ȫ����
D��ͨ����ĵ缫Ϊ��ظ����������ĵ缫��ӦΪ��C3H8-20e-+10O2-=3CO2+4H2O
�ο��𰸣�A�������ڵ�����У�O2-��������������A����
B������ȼ�ϵ�ص��ܷ�Ӧʽ�����ȼ�յķ���ʽ��ͬ����ΪC3H8+5O2=3CO2+4H2O����B��ȷ��
C��n��C3H8��=5.6L22.4L/mol=0.25mol��C3H8������ΪCO2�����ݻ��ϼ۵ı仯��֪��ת�Ƶ��ӵ����ʵ���Ϊ0.25mol��[3��4-��-8��]=5mol��Ҳ�ɸ��ݵ缫��Ӧʽ�жϣ���C��ȷ��
D����ع���ʱ�������ڸ������������缫����ʽΪC3H8-20e-+10O2-=3CO2+4H2O����D��ȷ��
��ѡA��
���������
�����Ѷȣ���
4��ѡ���� ��ͼ���ճ������г����綯���г���Ҫ����֮Ǧ���ؽṹʾ��ͼ���й�˵������ȷ����
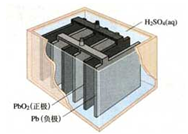
A��Ǧ�������ڶ��ε��
B��ʵ��ʹ�ù����п������γ�ŵ�
C��ʹ�ù����и�������������Ӧ
D��Ǧ�������������Ⱦ������������ĵ��
�ο��𰸣�B
���������Ǧ���ؿ��ظ���ŵ磬���ڶ��ε�أ�Ҳ���dz���أ��ŵ�ʱ����Ϊԭ��أ���������������Ӧ�����ڿ�������ؽ���Ǧ����Ⱦ�����Բ���������ĵ�أ�
���ų����������࣬��ص�������С����ص���������ص�����Խ��Խ���ѡ��B��������
�����Ѷȣ�һ��
5��ѡ���� ��п���Ե�صĵ������ҺΪŨKOH��Һ���ŵ�ʱ���ܷ�ӦΪ��
Ag2O2+2Zn+4KOH+2H2O=2K2Zn( OH )4+2Ag�����йظõ�ص�˵������ȷ����
A����طŵ�ʱ������������Һ�ļ�����ǿ
B����طŵ�ʱ��������ӦΪ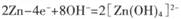
C����س��ʱ��������ӦΪ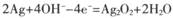
D�����ʱп�������Դ��������
�ο��𰸣�D
���������ԭ����и���ʧȥ���ӣ�����������Ӧ�������õ����ӣ�������ԭ��Ӧ�����Ը��ݷŵ���ܷ���ʽ��֪�����������ĵ缫��Ӧʽ�ֱ���Ag2O2+4e����2H2O��2Ag��4OH����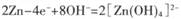 ������ѡ��AB������ȷ�ġ�����൱���Ƿŵ���淴Ӧ������ѡ��C��ȷ��D����ȷ��п��Ӧ�������Դ�ĸ���ѡ���ѡD��
������ѡ��AB������ȷ�ġ�����൱���Ƿŵ���淴Ӧ������ѡ��C��ȷ��D����ȷ��п��Ӧ�������Դ�ĸ���ѡ���ѡD��
�����Ѷȣ���