|
高中化学知识点讲解《物质的量》高频考点预测(2017年最新版)(四)
2017-11-11 02:08:18
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、选择题 用Na2CO3固体配制一定物质的量浓度的Na2CO3溶液时,不需要使用的玻璃仪器是
A.容量瓶
B.玻璃棒
C.漏斗
D.烧杯
|
参考答案:C
本题解析:用Na2CO3固体配制一定物质的量浓度的Na2CO3溶液时,需要使用的玻璃仪器是烧杯溶解物质,用玻璃棒搅拌促进物质的溶解,并用玻璃棒引流溶液到容量瓶中,没有使用的是漏斗,故选项是C。
考点:考查物质的量浓度的溶液配制时仪器的使用的知识。
本题难度:一般
2、选择题 NA表示阿伏加德罗常数的值,下列说法正确的是
①用铜作电极电解饱和NaCl溶液,当线路中通过NA个电子时,阳极产生11.2L气体(标准状况下)
②常温常压下,16gO2和16gO3含氧原子数均为NA
③标准状况下,22.4? L CH3CH2OH中含有的碳原子数为2NA
④6.5g锌全部溶于一定量的浓硫酸,生成SO2与H2的混合气体,气体分子总数为0.1 Na
⑤106gNa2CO3粉末中含有CO32-数为NA
A.②④⑤
B.①③⑤
C.①②④⑤
D.①②③
参考答案:A
本题解析:
试题解析:用Cu作电极电解饱和食盐水,Cu是活泼电极,阳极电极失电子,不会产生气体,①错;O2、O3均由O原子构成,16g O2、O3含有的O原子数均为NA,②正确;乙醇标准状况下是液体,无法用气体摩尔体积计算,③错;Zn与浓硫酸反应时,会生成SO2气体,若浓硫酸变稀,还会发生Zn与稀硫酸的反应,生成H2,无论哪个反应,根据方程式可知,转移电子数为2mol时,生成气体1mol,6.5g Zn的物质的量为0.1mol,反应失去电子0.2mol,则生成的气体分子数为0.1mol,④正确;Na2CO3晶体属于离子晶体,每个分子由2个Na+和1个CO32-构成,106g Na2CO3粉末的物质的量为1mol,则含有CO32-数为NA,⑤正确。
本题难度:一般
3、选择题 已知溶质质量分数为96%的酒精溶液的物质的量浓度为16.6 mol・L-1,试判断48%的酒精溶液的物质的量浓度(mol・L-1)(已知酒精的密度小于1)
[? ]
A.大于8.3
B.等于8.3
C.小于8.3
D.无法确定
参考答案:A
本题解析:
本题难度:一般
4、填空题 1 (6分)有以下几种物质
①乙醇?②MgCl2晶体?③蔗糖?④铜?⑤食盐水?⑥BaSO4?
请填空回答(填序号)。
(1)以上物质中能导电的是?;
(2)以上物质中属于电解质的是?;
(3)以上物质中属于非电解质的是?。
2.(4分)现有CO和CO2的混合气体18g,充分与氧气反应后测得所得到的CO2的总体积为11.2L(标准状况)。试计算
(1)原混合气体中CO2的体积(标准状况)是?,
(2)原混合气体在标准状况下的密度是??g/L (结果保留一位小数)
参考答案:1? (1)④⑤?(2)②⑥? (3)①③
2.(1)5.6L;?(2)1.6g/L
本题解析:1、铜为单质、食盐水为混合物,既不是电解质,也不是非电解质;
酸碱盐均为电解质,故MgCl2晶体、BaSO4为电解质
乙醇与蔗糖在水溶液中和熔融状态下均不能导电,为非电解质
有自由电子及活动的自由离子的物质可导电,包括铜及食盐水
2、设原气体中CO、CO2的物质的量为x、y,则28x+44y=18
由反应2CO+O2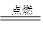 2CO2可知,最终所得到的CO2的总体积为22.4(x+y)=11.2 2CO2可知,最终所得到的CO2的总体积为22.4(x+y)=11.2
解得x=y=0.25mol
故原混合气体中CO2的体积(标准状况)是0.25×22.4=11.2L
原混合气体在标准状况下的密度是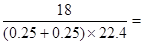 1.6g/L 1.6g/L
本题难度:一般
5、选择题 8.下列物质溶于水电离出的Cl―数目与2molNaCl溶于水电离出的Cl―数目相同的是( )
A.1molAlCl3
B.2molKClO3
C.1molMgCl2
D.1.5molCaCl2
|