|
高中化学知识点讲解《物质的量》答题技巧(2017年最新版)(四)
2017-11-11 02:10:15
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、选择题 一定条件下,使CO和O2的混合气体26 g充分反应,所得混合物在常温下跟足量的Na2O2固体反应,结果固体增加14 g,则原混合气体中CO和O2的物质的量之比是
A.4:9
B.1:1
C.7:6
D.4:3
|
参考答案:C
本题解析:
由反应2Na2O2+2CO2=2Na2CO3+O2,可知混合物在常温下跟足量的Na2O2固体反应生成固体为Na2CO3,1molNa2O2生成1molNa2CO3,质量增加28g,恰好为CO的质量,固体增重14g,说明混合气体中CO为14g,则O2为26g-14g=12g,所以原混合气体中CO和O2的质量比为
14g:12g =7:6。
考点:考查混合物的计算
点评:本题考查了混合物的相关计算,需要一定的观察能力,难度中等。解题时可以从物质的化学式组成上入手分析,可以大大简化理解和计算过程。
本题难度:一般
2、选择题 设NA为阿伏加德罗常数的值,下列有关叙述不正确的是(?)
A.标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为7/22.4NA
B.1 mol甲基(―CH3)所含的电子总数为9NA
C.0.5 摩1, 3-丁二烯分子中含有碳碳双键数为 NA
D.1 mol碳正离子(CH3+ )所含的电子总数为8NA
参考答案:A
本题解析:标准状况下,庚烷不是气体,即1L庚烷的物质的量不是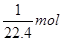 ,A不正确。甲基是中性的,所以1 mol甲基(―CH3)所含的电子总数为9NA。1, 3-丁二烯分子中含有2个碳碳双键,C正确。碳正离子带1个正电荷,所以1 mol碳正离子(CH3+ )所含的电子总数为8NA。答案是A。 ,A不正确。甲基是中性的,所以1 mol甲基(―CH3)所含的电子总数为9NA。1, 3-丁二烯分子中含有2个碳碳双键,C正确。碳正离子带1个正电荷,所以1 mol碳正离子(CH3+ )所含的电子总数为8NA。答案是A。
本题难度:一般
3、选择题 用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.1 L 1 mol・L-1的FeCl3溶液中含有NA个Fe3+
B.标准状况下,22.4 L己烷中共价键数目为19NA
C.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA
D.常温常压下的33.6 L氯气与27 g铝反应,转移电子数为3NA
参考答案:C
本题解析:略
本题难度:一般
4、选择题 用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.5.6g铁粉在2.24L(标准状态)氯气中充分燃烧,失去的电子数为0.3NA
B.常温下,1 molO2和O3的混合气体中所含氧原子数为2.5NA
C.CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等
D.13.0 g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2NA
参考答案:D
本题解析:A错,铁与氯反应的方程式为:2Fe+3CL2=2FeCL3;5.6g铁粉的物质的量为0.1mol;2.24L(标准状态)氯气物质的量为0.1mol;即氯气的量不足,反应过程中失去的电子数为0.2NA;B错,由于不知道O2和O3的各自的物质的量,本题无解;C错,未指明标准状况;D正确,13.0 g锌的物质的量为0.2 mol;锌与浓硫酸反应或稀硫酸反应均为1 mol锌生成1 mol气体;
本题难度:一般
5、选择题 下列叙述错误的是( )
A.物质的量是国际单位制中七个基本物理量之一
B.0.016kg16O含有约6.02×1023个氧原子
C.一定温度、压强下,气体体积由其分子的数目决定
D.1mol氧的质量为16g
参考答案:D
本题解析:
本题难度:简单
|