1、计算题 (本题共14分)自然界中,金属硫化物矿床常因发生表生氧化及次生富集作用,产生辉铜矿(Cu2S)与铜蓝(CuS)。
已知:Cu2S、CuS是两种不溶于水的黑色固体,在一定条件下都能与稀HNO3反应:
①3CuS+8H++8NO3-→3Cu2++3SO42-+8NO↑+4H2O
②3Cu2S+16H++10NO3-→6Cu2++3SO42-+10NO↑+8H2O
现将四份质量不同的某Cu2S和CuS混合物样品分别与100mL 5mol/L的稀硝酸充分反应,样品质量与产生气体的体积(已折合成标准状况)如下表所示:
实验编号
| 甲
| 乙
| 丙
|
样品质量(g)
| 9.6
| 12.8
| 64.0
|
气体体积(L)
| 5.04
| 6.72
| V
|
试回答下列问题(不考虑硝酸的挥发以及溶液体积变化):
53.用质量分数为0.63、密度为1.42g/cm3的浓硝酸配置100mL、5mol/L的稀硝酸,需浓硝酸的体积为 。(保留1位小数)
54.甲实验结束后,溶液中c(NO3-) = 。
55.混合物样品中Cu2S、CuS的物质的量之比是多少?(写出计算过程)
56.乙实验结束后,溶液中氢离子的浓度是多少?(写出计算过程)
57.计算丙实验中产生气体的体积(V)。(写出计算过程)
参考答案:53、35.2mL (2分) 54、2.75mol/L (2分)
55、解:设12.8g的样品中CuS的物质的量为x ,Cu2S的物质的量为y
96x+160y=12.8
8x/3+10y/3=0.3
解得:x=y=0.05mol
根据方程式①、②可知消耗n(H+)=0.05mol×8/3+0.05mol×16/3=0.4mol
故剩余n(H+)=0.1mol,c(H+)=1mol/L (4分)
56、解:根据方程式①、②可知消耗n(H+)=0.05mol×8/3+0.05mol×16/3=0.4mol
故剩余n(H+)=0.1mol,c(H+)=1mol/L (2分)
57、解:首先判断64g样品中CuS、Cu2S的物质的量为0.25mol
若HNO3均与CuS反应:硝酸不足,则V(NO)=0.5mol×22.4L/mol=11.2L
若HNO3均与Cu2S反应:硝酸不足,则V(NO)=0.5mol×22.4L/mol=7L
所以:丙中产生气体体积(V):7L< V < 11.2L (4分)
本题解析:53、用质量分数为0.63、密度为1.42g/cm3的浓硝酸配置100mL、5mol/L的稀硝酸,需浓硝酸的体积为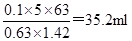 ;
;
54、根据甲、乙数据可知甲中硝酸过量,根据氮原子守恒可知被还原的硝酸的物质的量是5.04L÷22.4L/mol=0.225mol,则剩余硝酸根的物质的量是0.1L×5mol/L-0.225mol=0.275mol,剩余反应后溶液中c(NO3-) =0.275mol÷0.1L=2.75mol/L;
55、设12.8g的样品中CuS的物质的量为x ,Cu2S的物质的量为y
96x+160y=12.8
8x/3+10y/3=0.3
解得:x=y=0.05mol
根据方程式①、②可知消耗n(H+)=0.05mol×8/3+0.05mol×16/3=0.4mol
故剩余n(H+)=0.1mol,c(H+)=1mol/L
56、根据方程式①、②可知消耗n(H+)=0.05mol×8/3+0.05mol×16/3=0.4mol
故剩余n(H+)=0.1mol,c(H+)=1mol/L
57、首先判断64g样品中CuS、Cu2S的物质的量为0.25mol
若HNO3均与CuS反应:硝酸不足,则V(NO)=0.5mol×22.4L/mol=11.2L
若HNO3均与Cu2S反应:硝酸不足,则V(NO)=0.5mol×22.4L/mol=7L
所以:丙中产生气体体积(V):7L< V < 11.2L
考点:考查硝酸与铜的硫化物反应的有关计算
本题难度:困难
2、选择题 阿伏加德罗常数用NA表示,下列叙述正确的是?
A.18g D2O含有电子数为10 NA
B.NA个Fe(OH)3胶体粒子的质量为107 g
C.12g石墨中含有的σ键数目为3NA
D.常温常压下,S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2 NA
参考答案:D
本题解析:A.18g D2O是18/20mol含有电子数为不是10 NA,错误;B. 由于Fe(OH)3胶体粒子是由多个Fe(OH)3基团组成,故NA个Fe(OH)3胶体粒子的质量大于107 g,错误;C.12g石墨即1mol,由于1个碳中有1.5个中σ键,故数目为1.5NA,错误;D.S2和S8都是由硫原子构成,其混合物共6.4g,所含硫原子数是一定值,一定为0.2 NA,正确。A的相关判断和计算。
本题难度:一般
3、选择题 MgSO4和Al2(SO4)3溶液等体积混合后,铝离子的物质的量浓度为0.1mol/L,硫酸根离子的浓度为0.3mol/L,则混合液中镁离子的浓度为
[? ]
A.0.15mol/L
B.0.3mol/L
C.0.45mol/L
D.0.2mol/L
参考答案:A
本题解析:
本题难度:简单
4、选择题 由K2SO4、Al2(SO4)?3、KAl(SO4)?2・12H2O及H2SO4组成的混合溶液测得c(H+)?=0.1mol・L-1,c(Al 3+)="0.2" mol・L-1,c(SO42-)?="0.5" mol・L-1,则c(K+)为(?)
A.0.2 mol・L-1
B.0.3 mol・L-1
C.0.4 mol・L-1
D.0.5 mol・L-1
参考答案:B
本题解析:溶液不显电性,所以根据电荷守恒可以得到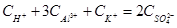 ,所以
,所以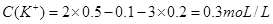 ,答案选B。
,答案选B。
本题难度:简单
5、填空题 (1)物质的量的符号是______单位是______;物质的量浓度的单位是______;在标准状况下,1mol任何气体的体积都约为______L.
(2)在标准状况下,448mL某气体的质量为0.64克,则该气体的物质的量是______;该气体的摩尔质量是______.(该小题计算正确但写错单位或不下单位各扣1分)
参考答案:(1)物质的量的符号是n,单位是摩尔;物质的量浓度的单位是mol/L;在标准状况下,1mol任何气体的体积都约为22.4L,
故答案为:n;摩尔;mol/L;22.4;
(2)标准状况下,448mL某气体的质量为0.64克,则该气体的物质的量是0.448L22.4L/mol=0.02mol,该气体的摩尔质量为0.64g0.02mol=32g/mol,
故答案为:0.02mol;32g/mol.
本题解析:
本题难度:一般