1、填空题 某小组的同学对放置已久的过氧化钠的成份进行探究,请回答下列问题:
(1)反应?2Na2O2+2H2O=4NaOH+O2↑的还原剂是______(写化学式);反应2Na2O2+2CO2=2Na2CO3+O2↑中,每生成1molO2则转移了______mol电子.
(2)进行探究:
①提出假设.?假设1:全部是Na2O2?假设2:全部是Na2CO3 假设3:______
②设计方案,进行实验.请在答题卡上写出实验步骤以及预期现象和结论(可不填满).限选实验试剂和仪器:蒸馏水、1moL?L-1H2SO4、澄清石灰水、淀粉-KI溶液、酚酞溶液、火柴、试管、小烧杯.
| 实验步骤 | 预期现象和结论
步骤1:取少量固体样品于试管中,滴加足量1moL?L-1?H2SO4至固体溶解,然后将内壁附有澄清石灰水的烧杯罩于试管口.
若澄清石灰水未见浑浊,则假设1成立;
若澄清石灰水变浑浊,则______
______
步骤2:
步骤3:
参考答案:因Na2O2在反应中既是氧化剂又时还原剂,因反应2Na2O2+2CO2=2Na2CO3+O2↑中2个Na2O2转移2个电子,每生成1molO2则转移了2mol电子,故答案为:Na2O2;2;?
(2)①也可能是两者的混合物,故答案为:是Na2O2与Na2CO3的混合物
②因Na2O2与硫酸反应产生氧气,Na2CO3与与硫酸反应产生二氧化碳,Na2O2具有漂白性来解答,故答案为:实验步骤预期现象和结论假设2或假设3成立,或假设1不成立步骤2:另取少量固体于试管中加适量蒸馏水,再滴入酚酞溶液若滴入酚酞溶液后先变红后褪色则假设1或假设3成立;若红色不褪色,则假设2成立
本题解析:
本题难度:一般
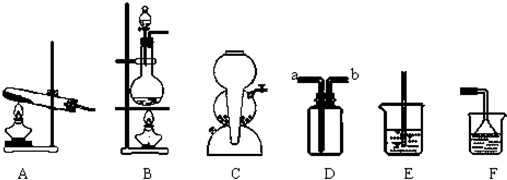
2、选择题 下列所示的实验装置能达到实验目的的是
[? ]
A.制取氨气 
B.测定化学反应速率 
C.稀释浓硫酸 
D.比较KMnO4、Cl2、S的氧化性 
参考答案:D
本题解析:
本题难度:一般
3、选择题 下表中实验操作不能达到实验目的的是
[? ]
实验操作
实验目的
A.
加新制的Cu(OH)2并加热
检验糖尿病人尿液中是否含有葡萄糖
B.
通入稀溴水
检验SO2中是否混有乙烯
C.
滴入紫色石蕊试液?
检验酒精中是否混有醋酸
D.
用饱和碳酸钠溶液洗涤后分液
除去乙酸乙酯中少量的乙醇和乙酸
参考答案:B
本题解析:
本题难度:一般
4、简答题 有一包白色粉末,可能由KCl、BaCO3、BaCl2、KNO3、NH4NO3和Na2SO4中的一种或几种组成.现进行下列实验:
(1)将此粉末溶于水中,得到无色透明溶液A及白色沉淀B,过滤.
(2)取沉淀物B,加稀HNO3后,沉淀物B不溶解.
(3)取少量溶液A,加入适量的NaOH溶液,加热,产生无色有刺激性气味并能使湿润的红色石蕊试纸变蓝色的气体.
(4)再取少量溶液A,滴入AgNO3溶液,充分反应后,有白色沉淀生成,该沉淀不溶于稀硝酸.
据此推断,该白色粉末中,一定含有______,肯定不含有______,可能含有______.
参考答案:(1)将此粉末溶于水中,得到无色透明溶液A及白色沉淀B,该沉淀可能为BaCO3或BaSO4,或二者都有;
(2)取沉淀物B,加稀HNO3后,沉淀物B不溶解,说明沉淀为BaSO4,不含BaCO3,则一定有BaCl2和Na2SO4;
(3)取少量溶液A,加入适量的NaOH溶液,加热,产生无色有刺激性气味并能使湿润的红色石蕊试纸变蓝色的气体,生成的气体为氨气,则应含有NH4NO3;
(4)再取少量溶液A,滴入AgNO3溶液,充分反应后,有白色沉淀生成,该沉淀不溶于稀硝酸,该沉淀为AgCl,由于含有,则不能确定是否有KCl;
由于和任何物质都不反应,则不能确定是否有KNO3,
则一定含有:BaCl2、Na2SO4、NH4NO3;肯定不含有:BaCO3;可能含有:KCl、KNO3,
故答案为:BaCl2、Na2SO4、NH4NO3;BaCO3;KCl、KNO3.
本题解析:
本题难度:一般
5、填空题 (1)实验室用食盐晶体与浓硫酸在微热条件下反应制取氯化氢气体,反应的化学方程式为______.
(2)氯化氢气体的发生装置应该选择装置______(填装置的编号,下同).由于氯化氢气体有毒,所以实验室用装置D来收集氯化氢,则收集氯化氢时,气体从______管(填a或b)进入.用水吸收多余的氯化氢气体时,应该选择装置______,这是为了防止______.
(3)要得到干燥的氯化氢气体,还需要在制取和收集装置之间插入一个干燥装置D,此时D中装入的液体应该是______.
(4)为了比较盐酸溶液与氯化氢气体性质的不同之处,取两支试管,一支滴入2~3mL盐酸,另一支收集干燥的氯化氢气体并塞好橡皮塞,然后各放入一片干燥的蓝色石蕊试纸.观察到的现象是______.再取两支试管,一支滴入2~3mL盐酸,另一支收集干燥的氯化氢气体并塞好橡皮塞,然后各放入一小块锌片.观察到的现象是______.
参考答案:(1)实验室用食盐晶体与浓硫酸在微热条件下反应制取氯化氢气体,反应生成氯化氢气体和硫酸氢钠,反应的化学方程式为NaCl(s)+H2SO4(浓)微热.NaHSO4+HCl↑,故答案为:NaCl(s)+H2SO4(浓)微热.NaHSO4+HCl↑;
(2)实验室利用二氧化锰和浓盐酸加热反应生成氯化锰,氯气和水,是固体+固体△.气体,选择装置B;氯化氢是比空气重的极易溶于水的气体需要用向上排气法收集,导气管长进短处,应从a处进,多余的氯化氢气体用水吸收要防止倒吸,应选择装置F防止水倒吸入集气瓶,
故答案为:B;a;F;水倒吸入集气瓶;
(3)装置D干燥气体是利用洗气,应选择液体干燥剂,能用于干燥氯化氢气体的干燥剂选择浓硫酸,故答案为:浓硫酸;
(4)盐酸是氯化氢气体的水溶液电离出氢离子显酸性,干燥的氯化氢是氯化氢分子无氢离子,各放入一片干燥的蓝色石蕊试纸,盐酸溶液中石蕊试纸变红色,干燥的氯化氢气体中试纸无变化,各放入一小块锌片,盐酸中锌片溶解,反应生成氢气,氯化氢气体中无变化,
故答案为:盐酸中石蕊试纸变红,干燥氯化氢中试纸不变色,盐酸中锌片溶解,有气泡产生,氯化氢中锌片无变化.
本题解析:
本题难度:简单
|