1、选择题 某校学生用化学知识解决生活中的问题,下列家庭小实验不合理的是
[? ]
A.用食醋除去暖水瓶中的薄层水垢
B.米汤检验含碘盐中的碘酸钾(KIO3)
C.用食用碱(Na2CO3)溶液洗涤餐具上的油污
D.灼烧并闻气味的方法区别纯棉织物和纯毛织物
参考答案:B
本题解析:
本题难度:一般
2、选择题 某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
据此可以推断:该溶液中肯定不存在的离子组是?
[?]
A.Al3+、Mg2+、I-、SO32-?
B.Mg2+、Na+、CO32-、I-
C.Al3+、Na+、SO32-、I-?
D.Al3+、CO32-、Br-、SO32-
参考答案:A
本题解析:
本题难度:一般
3、选择题 可以肯定溶液中大量存在SO42-的实验事实是( )
A.加入氯化钡溶液时有白色沉淀,再加硝酸,沉淀不消失
B.加入硝酸溶液,无明显现象,再加入氯化钡溶液时有白色沉淀
C.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失?
D.加入足量盐酸无明显现象,再滴加氯化钡溶液有白色沉淀?
参考答案:A、滴加BaCl2溶液不能排除银离子的干扰,氯化银难溶于硝酸,故A错误;
B、先加入硝酸不能排除亚硫酸根离子的干扰,亚硫酸根离子易被硝酸氧化为硫酸根离子而生成硫酸钡沉淀,故B错误;
C、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,不能排除银离子的干扰,氯化银难溶于硝酸,故C错误;
D、先加入稀盐酸,没有产生沉淀,排除银离子的干扰,然后再加氯化钡,产生白色沉淀,证明有SO42-存在,故D正确;
故选D.
本题解析:
本题难度:一般
4、填空题 (1)有下列操作供选择:
A.加NaOH溶液 B.加盐酸 C.加硝酸 D.加热 E.加AgNO3溶液 F.加水过滤 G.加MnO2 H.置于空气中(填序号,可以重复选择)
证明一种金属粉末是铁粉的操作顺序是____________。
证明KClO3中含有氯元素的操作顺序是____________。
(2)亚硝酸钠NaNO2可用作水泥施工的抗冻剂。它易溶于水,有碱味,有氧化性,也有还原性。在酸性溶液中它能氧化碘离子、亚铁离子。它能将人体内血红蛋白里所含有亚铁离子氧化为三价铁离子使人中毒,在建筑工地上多次发生把硝酸钠误作食盐使用,导致民工中毒的事件。亚硝酸钠和酸反应应生产亚硝酸,亚硝酸是不稳定的弱酸,它只存于冷的稀溶液中,易发生如下分解反应。3HNO2=2NO↑+HNO3+
H2O从醋酸、氨水、纯碱、稀盐酸、碘化钾淀粉溶液中选择适当的物质做试剂,用两种简单的化学实验方法来鉴别亚硝酸钠和氯化钠。
方法一:试剂是(只用一种试剂)____________;现象:____________。
方法二:实验步骤及实验现象是__________________________________。
参考答案:(1)BAH;GDFCE
(2)方法一:稀盐酸;加盐酸后微热,若有气泡产生,且气体遇空气后变红棕色则为亚硝酸钠,无现象则为氯化钠
方法二:取适量试样于试管中,加入KI-淀粉溶液和醋酸,若溶液变蓝色,则为NaNO2,无现象则为氯化钠
本题解析:
本题难度:一般
5、选择题 用试纸检验气体性质是一种重要的实验方法。如图所示的实验中(可以加热),下列试纸的选用、现象、对应结论都正确的一项是
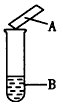
[? ]
试剂B?
湿润的试纸A
?现象
?结论
A.
碘水?
淀粉试纸
变蓝
?碘具有氧化性
B.
浓氨水,生石灰?
蓝色石蕊试纸
变红
?氨气为碱性气体
C.
Na2SO3,硫酸?
品红试纸
褪色
SO2具有漂白性
D.
Cu,浓硝酸?
?KI淀粉试纸
变蓝
NO2为酸性气体
参考答案:C
本题解析:
本题难度:简单