1、选择题 下列离子方程式中书写正确的是( )
A.铝与盐酸反应Al+H+═Al3++H2↑
B.硫酸铜与Ba(OH)2溶液反应Cu2++2OH-═Cu(OH)2↓
C.铁与FeCl3溶液反应Fe+Fe3+═2Fe2+
D.硝酸银溶液与氯化钠溶液反应Ag++Cl-═AgCl↓
参考答案:A.铝与盐酸反应的离子反应为2Al+6H+═2Al3++3H2↑,故A错误;
B.硫酸铜与Ba(OH)2溶液反应的离子反应为SO42-+Ba2++Cu2++2OH-═Cu(OH)2↓+BaSO4↓,故B错误;
C.铁与FeCl3溶液反应的离子反应为Fe+2Fe3+═3Fe2+,故C错误;
D.硝酸银溶液与氯化钠溶液反应的离子反应为Ag++Cl-═AgCl↓,故D正确;
故选D.
本题解析:
本题难度:简单
2、选择题 下列方程式书写正确的是
A.碳酸的电离方程式:H2CO3 2H+ + CO32-
2H+ + CO32-
B.向氯化钙溶液中通入二氧化硫气体:Ca2+ + SO2 + H2O = CaSO3 ↓+ 2H+
C.往AgI悬浊液中滴加Na2S饱和溶液: 2Ag+ (aq)+ S2-(aq) = Ag2S(s)
D.明矾水解:Al3+ + 3H2O  Al(OH)3+ 3H+
Al(OH)3+ 3H+
参考答案:D
本题解析:碳酸为两元弱酸,所以的电离方程式:H2CO3 ?H+ + HCO3-,HCO3-
?H+ + HCO3-,HCO3- H+ + CO32-,故A错误;向氯化钙溶液中通入二氧化硫气体并不能发生反应,因为盐酸的酸性比亚硫酸强,所以B错误;往AgI悬浊液中滴加Na2S饱和溶液的方程式应该为2AgI(s)+ S2-(aq) = Ag2S(s)+2I-,故C错误;D正确,明矾水解:Al3+ + 3H2O
H+ + CO32-,故A错误;向氯化钙溶液中通入二氧化硫气体并不能发生反应,因为盐酸的酸性比亚硫酸强,所以B错误;往AgI悬浊液中滴加Na2S饱和溶液的方程式应该为2AgI(s)+ S2-(aq) = Ag2S(s)+2I-,故C错误;D正确,明矾水解:Al3+ + 3H2O  ?Al(OH)3+ 3H+。
?Al(OH)3+ 3H+。
点评:本题考查了化学方程式的书写,属于对基础知识的考查,本题考查的都是学生熟悉的知识点,比较容易。
本题难度:简单
3、选择题 下列离子方程式书写正确的是?(?)
A?用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O
B. NaHSO4溶液中滴入Ba(OH)2溶液至中性? H++SO42-+Ba2++OH-=BaSO4↓+H2O
C.实验室用浓盐酸与MnO2反应制Cl2:MnO2 + 2H+ + 2Cl-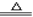 Cl2↑+ Mn2+ + H2O
Cl2↑+ Mn2+ + H2O
D.用FeCl3溶液腐蚀印刷电路板: Fe3+ + Cu?= Fe2+ + Cu2+
参考答案: A
A
本题解析:B项中性时应为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,错B;C错,原子不守恒;D项得失电子与电荷都不守恒,故D错。
本题难度:一般
4、选择题 下列离子方程式正确的是
A.向盐酸中滴加氨水:H++OH-=H2O
B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
C.铜溶于稀硝酸:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
D.Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+
参考答案:C
本题解析:A项:氨水的主要成分一水合氨是弱电解质,不能拆开,故错;B项:忽略了铁离子和碘离子的氧化还原反应,故错;D项:Cl2具有强氧化性能氧化SO32-成SO42-,故错。故选C。
点评:离子方程式正误判断要注意:看原则:看是否符合客观事实、看是否符合质量守恒、看是否符合电荷守恒、看是否符合得失电子相等。可溶的易电离的物质拆成离子。注意过量、少量、适量等。
本题难度:一般
5、选择题 下列反应的离子方程式正确的是(?)
A.硫酸钠稀溶液与三氧化硫反应:SO4 2-+SO3+H2O=2H++2SO42-
2-+SO3+H2O=2H++2SO42-
B.硫酸铝溶液和小苏打溶液混合:Al3++2HCO3-=3CO2+Al(OH)3
C.氯气和溴化钠反应:Cl2+2Br -=2Cl-+Br2
-=2Cl-+Br2
D.碳酸钡溶于醋酸:BaCO3+2CH3COOH=Ba2++2CH3COO-+ H2O+CO2
H2O+CO2
参考答案:C
本题解析:略
本题难度:一般